TNFSF11, или RANKL (от англ. Tumor necrosis factor ligand superfamily member 11; Receptor activator of nuclear factor kappa-B ligand) — мембранный белок, цитокин семейства факторов некроза опухоли. Продукт гена человека TNFSF11. Играет важную роль в метаболизме костной ткани, активируя остеокласты.
Функции
TNFSF11 (обозначается также RANKL) входит в многочисленное семейство факторов некроза опухоли (TNF). Является лигандом для рецепторов TNFRSF11B (остеопротегерин) и TNFRSF11A (RANK). Является ключевым фактором дифференцировки и активации остеокластов, клеток, которые обеспечивают резорбцию костной ткани. Кроме этого, RANKL играет роль в иммунной системе. Белок экспрессируется на Т-хелперах и вовлечён в созревание и выживание дендритных клеток. Активация Т-лимфоцитов приводит к индукции экспрессии цитокина, повышению остеокластогенеза и потере костной ткани. Кроме этого, RANKL активирует анти-апоптозную киназу AKT/PKB через комплекс Src-киназы и фактора TRAF6 и, таким образом, может играть роль в регуляции апоптоза.[1]
Структура
Белок состоит из 317 аминокислот, молекулярная масса — 35,5 кДа. Содержит небольшой N-концевой внутриклеточный домен, единственный трансмембранный участок и внеклеточный домен.
Является гомотримером. Является мембранным белком, но может высвобождаться в свободном виде после гидролиза участка 139-140 под действием протеазы ADAM17. При этом образуется белок из 178 аминокислот.
Взаимодействует с рецептором TNFRSF11B.
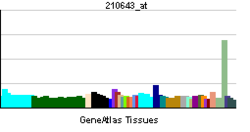
Тканевая экспрессия
Наивысшая экспрессия наблюдается в периферических лимфатических узлах, низкий уровень - в селезёнке, периферических лимфоцитах крови, костном мозге, сердце, плаценте, скелетных мышцах, желудке и щитовидной железе.
Роль в патологии
Избыточное продукция RANKL связана с рядом дегенеративных заболеваний, включая ревматоидный артрит и псориатический артрит.
Мутации гена TNFSF11 вызывают аутосомный рецессивный остеопетроз 2-го типа, нарушение костной ткани, характеризующееся повышенной плотностью из-за замедленной ресорбции незрелых костей.
См. также
Примечания
Литература
- Whyte M (2006). “The long and the short of bone therapy”. N Engl J Med. 354 (8): 860—3. DOI:10.1056/NEJMe068003. PMID 16495400. link
- Buckley KA, Fraser WD (2003). “Receptor activator for nuclear factor kappaB ligand and osteoprotegerin: regulators of bone physiology and immune responses/potential therapeutic agents and biochemical markers”. Ann. Clin. Biochem. 39 (Pt 6): 551—6. DOI:10.1258/000456302760413324. PMID 12564836.
- Jeffcoate W (2005). “Vascular calcification and osteolysis in diabetic neuropathy-is RANK-L the missing link?”. Diabetologia. 47 (9): 1488—92. DOI:10.1007/s00125-004-1477-5. PMID 15322748.
- Collin-Osdoby P (2005). “Regulation of vascular calcification by osteoclast regulatory factors RANKL and osteoprotegerin”. Circ. Res. 95 (11): 1046—57. DOI:10.1161/01.RES.0000149165.99974.12. PMID 15564564.
- Whyte MP, Mumm S (2005). “Heritable disorders of the RANKL/OPG/RANK signaling pathway”. Journal of musculoskeletal & neuronal interactions. 4 (3): 254—67. PMID 15615493.
- Clohisy DR, Mantyh PW (2005). “Bone cancer pain and the role of RANKL/OPG”. Journal of musculoskeletal & neuronal interactions. 4 (3): 293—300. PMID 15615497.
- Anandarajah AP, Schwarz EM (2006). “Anti-RANKL therapy for inflammatory bone disorders: Mechanisms and potential clinical applications”. J. Cell. Biochem. 97 (2): 226—32. DOI:10.1002/jcb.20674. PMID 16240334.
- Baud'huin M, Duplomb L, Ruiz Velasco C; et al. (2007). “Key roles of the OPG-RANK-RANKL system in bone oncology”. Expert Rev Anticancer Ther. 7 (2): 221—32. DOI:10.1586/14737140.7.2.221. PMID 17288531.
- Yogo K, Ishida-Kitagawa N, Takeya T (2007). “Negative autoregulation of RANKL and c-Src signaling in osteoclasts”. J. Bone Miner. Metab. 25 (4): 205—10. DOI:10.1007/s00774-007-0751-2. PMID 17593489.
- Boyce BF, Xing L (2007). “Biology of RANK, RANKL, and osteoprotegerin”. Arthritis Res. Ther. 9 Suppl 1: S1. DOI:10.1186/ar2165. PMC 1924516. PMID 17634140.
- McClung M (2007). “Role of RANKL inhibition in osteoporosis”. Arthritis Res. Ther. 9 Suppl 1: S3. DOI:10.1186/ar2167. PMC 1924518. PMID 17634142.
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .