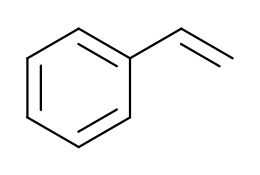
| Стирол | |
|---|---|
 | |
 | |
| Общие | |
| Хим. формула | C8H8 |
| Физические свойства | |
| Молярная масса | 104,15 г/моль |
| Плотность | 0,909 г/см³ |
| Энергия ионизации | 8,4 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | −30,6 °C |
| Т. кип. | 145 °C |
| Т. всп. | 88 ± 1 градус Фаренгейта[1] |
| Пр. взрв. | 0,9 ± 0,1 об.%[1] |
| Давление пара | 5 ± 1 мм рт.ст.[1] |
| Классификация | |
| Рег. номер CAS | 100-42-5 |
| PubChem | 7501 |
| Рег. номер EINECS | 202-851-5 |
| SMILES | |
| InChI | |
| RTECS | WL3675000 |
| ChEBI | 27452 |
| ChemSpider | 7220 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
В этой статье не хватает ссылок на источники информации. |
Стиро́л C8H8, C6H5CH=CH2, PhVi (фенилэтилен, винилбензол, этенилбензол) — бесцветная ядовитая жидкость со специфическим запахом. Стирол практически нерастворим в воде, хорошо растворим в органических растворителях, хороший растворитель полимеров. По гигиеническому нормативу ГН 2.1.6.3492-17 (содержание в воздухе населённых мест) стирол относится ко второму классу опасности, по классификации опасных грузов ООН - к третьему[2].
Получение
Большую часть стирола (около 85 %) в промышленности получают дегидрированием этилбензола:
при температуре 600—650 °С, атмосферном давлении и разбавлении перегретым водяным паром в 3—10 раз. Используются оксидные железо-хромовые катализаторы с добавкой карбоната калия.
Другой промышленный способ, которым получают оставшиеся 15 %, заключается в дегидратации метилфенилкарбинола, образующегося в процессе получения оксида пропилена из гидропероксида этилбензола. Гидропероксид этилбензола получают из этилбензола некаталитическим окислением воздухом.
Разрабатываются альтернативные способы получения стирола. Каталитическая циклодимеризация бутадиена в винилциклогексен, с его последующим дегидрированием. Окислительное сочетание толуола с образованием стильбена; метатезис стильбена с этиленом приводит к стиролу. Взаимодействием толуола с метанолом также может быть получен стирол. Кроме того, активно разрабатывались способы выделения стирола из жидких продуктов пиролиза. На сегодняшний день ни один из этих процессов не является экономически выгодным и в промышленном масштабе не реализован.
В лабораторных условиях может быть получен нагреванием до 320 °С полистирола с его моментальным отведением.
Свойства
Стирол легко окисляется, присоединяет галогены, полимеризуется (образуя твёрдую стекловидную массу — полистирол) и полимеризуется с различными мономерами. Полимеризация происходит уже при комнатной температуре (иногда со взрывом), поэтому при хранении стирол стабилизируют антиоксидантами (например, третбутилпирокатехином, гидрохиноном).
Галогенирование, например, в реакции с бромом, в отличие от анилина, идёт не по бензольному кольцу, а по виниловой группе с образованием (1,2-дибромэтил)бензола.
Применение
Стирол применяют почти исключительно для производства полимеров. Многочисленные виды полимеров на основе стирола включают полистирол, пенопласт (вспененный полистирол), модифицированные стиролом полиэфиры, пластики АБС (акрилонитрил-бутадиен-стирол) и САН (стирол-акрилонитрил). Также стирол входит в состав напалма.
Стружка из полистирола, растворённая в стироле, образует идеальный клей для полистирола: под действием тепла и остатков полимеризаторов клеевой шов достаточно быстро полимеризуется и полностью исчезает, таким образом 2 детали превращаются в единый монолит.
Токсичность
Стирол — яд общетоксического действия, он обладает раздражающим, мутагенным и канцерогенным эффектом и имеет очень неприятный запах (порог ощущения запаха — 0,07 мг/м³).
При хронической интоксикации у рабочих бывают поражены центральная и периферическая нервные системы, система кроветворения, пищеварительный тракт, нарушается азотисто-белковый, холестериновый и липидный обмен, у женщин происходят нарушения репродуктивной функции. Стирол проникает в организм в основном ингаляционным путём. При попадании на слизистые оболочки носа, глаз и глотки паров и аэрозоля стирол вызывает их раздражение. Содержание метаболитов бензола в моче — миндальной, фенилглиоксиновой, гинуриновой и бензойной кислот — используют в качестве экспозиционного теста.
Средняя летальная концентрация в воздухе составляет около 500—5000 мг/м³ (для крыс). Стирол относится к третьему классу опасности (по ГОСТ 10003-90).
Предельно допустимые концентрации (ПДК) стирола[3][4][5]:
Литература
- Нефтехимия. Доналд Л. Бардик, Уильям Л. Леффлер. М: Олимп-Бизнес, 2005
Примечания
- 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0571.html
- ↑ ICSC0073
- ↑ s:Гигиенические нормативы ГН 2.2.5.1313—03. «Предельно допустимые концентрации (ПДК) вредных веществ воздухе рабочей зоны».
- ↑ s:Гигиенические нормативы ГН 2.1.6.1338—03. «Предельно допустимые концентрации (ПДК) загрязняющих веществ в атмосферном воздухе населённых мест».
- ↑ s:Гигиенические нормативы ГН 2.1.5.1315—03. «Предельно допустимые концентрации (ПДК) химических веществ в воде водных объектов хозяйственно-питьевого и культурно-бытового водопользования».
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .
![{\displaystyle {\mathsf {C_{6}H_{5}C_{2}H_{5}{\xrightarrow[{}]{T}}C_{6}H_{5}CH=CH_{2}+H_{2}\uparrow }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/89c55a1089df3751c6830026fd0e68138430f189)