| Хлорпикрин | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
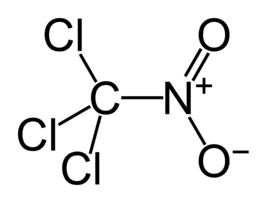
Хлорпикрин, нитрохлороформ, трихлорнитрометан |
| Хим. формула | CCl3NO2 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 164,376 г/моль |
| Плотность | 1,6539 (+20 °C) |
| Термические свойства | |
| Т. плав. | −69 °C |
| Т. кип. | 112,3 °C |
| Давление пара | 18 ± 1 мм рт.ст.[1] |
| Классификация | |
| Рег. номер CAS | 76-06-2 |
| PubChem | 6423 |
| Рег. номер EINECS | 200-930-9 |
| SMILES | |
| InChI | |
| RTECS | PB6300000 |
| ChEBI | 39285 |
| Номер ООН | 1580 |
| ChemSpider | 13861343 |
| Безопасность | |
| Токсичность |
высокотоксичен, ирритант, лакриматор  |
| NFPA 704 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Хлорпикри́н (трихлорнитрометан) CCl3NO2 — жидкость с резким раздражающим запахом; технический продукт может иметь различные оттенки запаха в зависимости от чистоты и способа получения. Используется как компонент фумигантных смесей в сельском хозяйстве[2], в камерах газоокуривания для проверки герметичности изолирующих и фильтрующих противогазов.
Методы синтеза
Хлорпикрин впервые получил шотландский химик Джон Стенхауз ещё в 1848 году при взаимодействии 2,4,6-тринитрофенола (пикриновой кислоты) с хлорной известью. Позднее этот старинный процесс был использован в промышленных процессах, при помощи которых в первую мировую войну хлорпикрин получали для военных целей. Действие гипохлоритов кальция (то есть дешёвой хлорной извести) приводит к расщеплению цикла 2,4,6- тринитрофенола и одновременно к хлорированию продуктов расщепления.
Вместо труднорастворимой пикриновой кислоты применяли легкорастворимый пикрат кальция, который получали смешением пикриновой кислоты с окисью кальция, и к смеси добавляли кашицу хлорной извести. Теплоты этой реакции достаточно для испарения образующегося хлорпикрина, пары которого затем конденсируют. Затем хлорпикрин легко перегоняется с водяным паром для очистки.
В реакции можно использовать не только хлорную известь, но другие гипохлориты — в том числе и образующиеся in situ при пропускании хлора в щелочной раствор пикриновой кислоты, либо других нитрофенолов.
В настоящее время основным промышленным способом синтеза хлорпикрина является хлорирование нитрометана в щелочной среде:
Хлорпикрин может также быть синтезирован нитрованием хлороформа ацетилнитратом:
Физико-химические свойства
Хлорпикрин — бесцветная, маслянистая, сильно преломляющая свет жидкость с резким специфическим запахом. На свету он становится зеленовато-желтоватым, что можно объяснить частичным его разложением с образованием хлора и окислов азота. Температура кипения 112—113 °C (760 мм рт. ст.) и +49 °C (40 мм рт. ст.), температура плавления — +62,2 (+64) °С.
Зависимость давления пара, максимальной концентрации от давления.
| Температура, °C | Давление пара, мм рт. ст. | Максимальная концентрация, мг/л |
|---|---|---|
| 0 | 5,91 | 57 |
| 10 | 10,87 | 104 |
| 20 | 16,91 | 184 |
| 30 | 30,50 | 295 |
Широкий температурный интервал, в котором хлорпикрин существует в жидком состоянии, и его высокая летучесть даже при низких температурах позволяет применять его в любое время года. В зимние месяцы достигается концентрация, меньшая абсолютно токсичной, но достаточная для подавления противника.
Стойкость на местности, лишённой растительности, составляет при обычной температуре около 6 часов. В этот период выход на заражённую местность или её преодоление без противогаза невозможны. Растворимость в воде при +25 °C, составляет 0,16 %. Хлорпикрин хорошо растворим в органических растворителях.
Из неорганических растворителей он хорошо растворяется в четырёххлористом кремнии и олове. Следует отметить, что хорошая смешиваемость с ОВ, например с ипритом, азотистым ипритом, дифосгеном, фосгеном, фосфорорганическими ОВ, делает хлорпикрин важным компонентом для тактических смесей, особенно в случае сравнительно низкоплавких ОВ, в результате чего становится возможным их применение в зимнее время.
Водой хлорпикрин не гидролизуется. Хлорпикрин легко дегазируется спиртовым раствором сульфида натрия, или растворами гидразина.
Хлорпикрин при высоком давлении и нагревании превращается в фосген.
Токсические свойства
Хлорпикрин раздражает кожу и слизистые оболочки. Он вызывает слезотечение, смыкание век, бронхит и отёк лёгких. У поражённого начинаются сильнейшие неконтролируемые конвульсии мышц диафрагмы. Жидкий хлорпикрин вызывает тяжёлые поражения кожи.
У большинства людей концентрация 0,002 мг/л за 3—30 с вызывает слезотечение и смыкание век, концентрация 0,05 мг/л — непереносима. Более высокие концентрации ведут к болям в области желудка, рвоте и потере сознания. Концентрация около 0,2 мг/л за несколько секунд или минут приводит к полной утрате боеспособности. Опасность хлорпикрина проявляется в том, что до некоторого предела концентрации он воспринимается на запах просто как умеренно пахнущее горчицей вещество, описанные выше симптомы поражения возникают внезапно.
Поражение органов дыхания появляется при концентрации выше 0,1 мг/л. В качестве смертельной концентрации указывают 2 мг/л при экспозиции 10 мин. При такой концентрации смерть наступает в течение нескольких минут.
Хлорпикрин как боевое отравляющее вещество (ОВ)
Пары хлорпикрина обладают сильным слезоточивым, а в высоких концентрациях — удушающим и общеядовитым действием. В связи с этим хлорпикрин ограниченно применялся в Первой мировой войне как боевое отравляющее вещество (например, против русской армии летом 1915 года), а также в качестве растворителя для боевого применения других БОВ (впервые — в середине 1916 года немецкой армией в смеси с дифосгеном).
Во время подавления антибольшевистского восстания в Тамбовской губернии зафиксировано три случая применения снарядов типа АЖО с хлорпикрином для выкуривания повстанцев из леса, не приведшие к заметным результатам[3].
Из-за невысокой для современных ОВ токсичности и сильного раздражающего действия хлорпикрин не рассматривается как боевое ОВ. С другими ОВ хлорпикрин также в настоящее время не используется, поскольку его раздражающее действие практически сразу дало бы возможность обнаружить применение ОВ.
Благодаря раздражающему действию и простоте обращения хлорпикрин используется в качестве учебного (имитация газовой атаки) и проверочного (тестирование средств химзащиты) ОВ. Для этого в армейской палатке умеренное количество хлорпикрина, порядка 50 мл, подогревается на водяной бане. Однако из-за того, что при нагревании хлорпикрин разлагается с образованием фосгена, применение его в качестве учебного ОВ требует соблюдения мер предосторожности. В связи с этим в настоящее время хлорпикрин как учебное ОВ постепенно заменяется другими ОВ раздражающего действия.
Ссылки
- Chloropicrin // «PubChem Compound» (англ.)
Примечания
- ↑ http://www.cdc.gov/niosh/npg/npgd0132.html
- ↑ Whitacre, David M. Reviews of Environmental Contamination and Toxicology /. — Springer, 2009-08-19. — ISBN 1441900276, 9781441900272.
- ↑ Aleksandr V. Glushko, Natal'ya I. Shilo “Clear the Woods the Thugs are Hiding in With Poisonous, Asphyxiating, Gases …”: Myths and Facts about the Tambov Uprising Voennyi Sbornik, 2013, № 2, pp. 103-125.
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .



