| Аспарагин | |
|---|---|
 | |
  | |
| Общие | |
| Систематическое наименование |
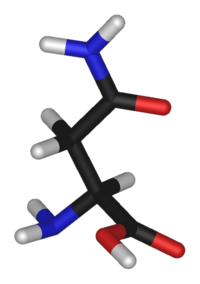
2-амино-3-карбамоилпропановая кислота |
| Сокращения |
Асн, Asn, N AAU,AAC |
| Традиционные названия | аспарагин |
| Хим. формула | HOOC-CH(NH2)-CH2-CONH2 |
| Рац. формула | C4H8N2O3 |
| Физические свойства | |
| Состояние | твёрдое |
| Примеси | L, D, LD |
| Молярная масса | 132,12 г/моль |
| Термические свойства | |
| Т. плав. | 220 моногидрат, 233 L, 182 LD |
| Химические свойства | |
| pKa | 2,02 и 8,84 |
| Растворимость в воде | растворим в воде |
| Вращение [α]D | + 21° |
| Изоэлектрическая точка | 5,41 |
| Классификация | |
| Рег. номер CAS | [70-47-3] |
| PubChem | 236 |
| SMILES | |
| InChI | |
| ChEBI | 22653 |
| ChemSpider | 231 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Аспараги́н (англ. Asparagine; принятые сокращения: Асн, Asn, N) — амид аспарагиновой кислоты (2-амино-бутанамид-4-овая кислота, Asx или B). Одна из 20 наиболее распространённых аминокислот природного происхождения. Их кодоны AAU и AAC.
История
Аспарагин был выделен из сока спаржи (англ. Asparagus) в 1806 году французским химиком Луи-Никола Вокленом и помощником Пьером Жаном Робике[1], став первой полученной человеком аминокислотой. В составе спаржи аспарагин содержится в больших количествах, соответственно он получил своё имя. Характерный запах мочи некоторых людей после употребления спаржи относят к различным метаболитам аспарагина[2]. Несколько лет позже, в 1809, Робике[1] снова обнаружил в корне лакрицы вещество похожее на аспарагин, затем Plisson в 1828 подтвердил это.
Бетаиновая структура
Аспарагин легко образует внутреннюю соль — бетаин.

Благодаря наличию хирального центра, существуют два энантиомера (S) и (R), участвующих в построении белков, и их смеси, вплоть до смеси с равным количеством — рацемат.
Так как в аспарагине боковые ответвления в виде карбоксамидной группы могут образовывать водородные связи с пептидной цепью, аспарагиновые остатки часто находят в начале и конце пептидной цепи, что характерно как для альфа-спирали, так и для β-листов[3]. Его роль может быть обозначена как «закупорка» водородных связей взаимодействием с концевыми группами, которые в других случаях могли бы связываться с основной полипептидной цепью. Глутамины с дополнительной метиленовой группой имеют большую конформационную энтропию, из-за чего они менее полезны в этом отношении. Аспарагин также обеспечивает реакции гликозилирования с образованием N-связанных гликанов (см. гликопротеины).
Свойства
С XIX века известны обе формы аспарагина. L-аспарагин имеет сладкий вкус, D-аспарагин — напротив, горький. Находящийся в пище сахар при его нагревании[4] с аспарагином образует акриламид — потенциальный канцероген.
Нахождение в природе
Аспарагин не является незаменимой аминокислотой (не требуется в диете), что означает способность человека синтезировать его основными метаболитическими путями. Он находится в значительных количествах в животных (молоко, сыворотка, мясо, птица, яйца, рыба, морепродукты) и растительных (спаржа, помидор, бобовые, орехи, семена, соя, цельные зёрна) источниках.
В живых клетках присутствует в свободном виде и в составе белков. Путём образования аспарагина из аспарагиновой кислоты в организме связывается токсический аммиак.
Биосинтез
Прекурсором аспарагина является оксалоацетат. Оксалоацетат конвертируется в аспартат энзимом трансаминазой, который переносит аминогруппу с глутамата на оксалоацетат, в результате чего образуются α-кетоглутарат и аспартат. А реакцию образования аспарагина, АМФ, глутамата и пирофосфата из аспартата, глутамина и АТФ катализирует аспарагинсинтетаза. В этой реакции АТФ активирует аспартат, образуя формил-β-аспартил-АМФ, а глутамин даёт аминогруппу, которая реагирует с β-аспартил-АМФ, образуя аспарагин и свободную АМФ.
Расщепление
L-аспарагиназа гидролизует амидную группу, образуя аспартат и аммиак. Аспартат — это глюкогенная аминокислота. Трансаминаза конвертирует аспартат в оксалоацетат, который может быть далее использован в цикле трикарбоновых кислот или глюконеогенезе.
Функция
Аспарагин требуется для нормального функционирования нервной системы. Он также играет важную роль в синтезе аммиака.
Примечания
- 1 2 en:Pierre Jean Robiquet
- ↑ [S.C. Mitchell (2001). «Food Idiosyncrasies: Beetroot and Asparagus». Drug Metabolism and Disposition 29: 539—534. Retrieved january 18, 2010.]
- ↑ uk:Бета-лист
- ↑ Вездесущая реакция Майара // Химия и жизнь №2, 2012.
Ссылки
- Аспарагин // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907. Статья Палладина В. И.
- Аспарагин, или амидосукцинаминовая кислота // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .