| Гистидин | |
|---|---|
 | |
 | |
| Общие | |
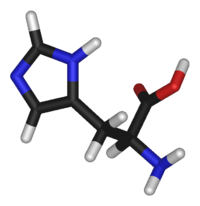
| Систематическое наименование |
L-2-амино-3-(1H-имидазол- 4-ил) пропановая кислота |
| Сокращения |
Гис, His, H CAU,CAC |
| Хим. формула | C₆H₉N₃O₂ |
| Рац. формула | C6H9N3O2 |
| Физические свойства | |
| Молярная масса | 155,16 г/моль |
| Термические свойства | |
| Т. плав. | 287 °C |
| Химические свойства | |
| pKa |
1,70 6,04 9,09 |
| Классификация | |
| Рег. номер CAS |
71-00-1 (L-гистидин) 351-50-8 (D-гистидин) 4998-57-6 (DL-гистидин) |
| PubChem | 6274 |
| Рег. номер EINECS | 200-745-3 |
| SMILES | |
| InChI | |
| ChEBI | 15971 |
| ChemSpider | 6038 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Гистиди́н (L-α-амино-β-имидазолилпропионовая кислота) — гетероциклическая альфа-аминокислота, одна из 20 протеиногенных аминокислот. Является одной из двух условно-незаменимых аминокислот (наряду с аргинином). Незаменимой является только для детей.
Гистидин растворим в воде, ограниченно растворим в этаноле, не растворим в эфире.
Химические свойства
Гистидин — ароматическая альфа-аминокислота со слабыми основными свойствами, обусловленными присутствием в молекуле остатка имидазола. Образует окрашенные продукты в биуретовой реакции и с диазотированной сульфаниловой кислотой (реакция Паули), что используется для количественного определения гистидина. Вместе с лизином и аргинином гистидин образует группу осно́вных аминокислот. Образует бесцветные кристаллы.
Содержание в продуктах
Гистидином богаты такие продукты как тунец, лосось, свиная вырезка, говяжье филе, куриные грудки, соевые бобы, арахис, чечевица. Кроме того, гистидин включается в состав многих витаминных комплексов и некоторых иных медикаментов.
Роль в организме
Остаток гистидина входит в состав активных центров множества ферментов. Гистидин является предшественником в биосинтезе гистамина. Одна из незаменимых аминокислот, способствует росту и восстановлению тканей. В большом количестве содержится в гемоглобине; используется при лечении ревматоидных артритов, язв и анемии. Недостаток гистидина может вызвать ослабление слуха.
Обмен гистидина
Дезаминирование гистидина происходит в печени и коже под действием фермента гистидазы с образованием уроканиновой кислоты, которая затем в печени превращается в имидазолонпропионовую кислоту под действием уроканиназы. Дальнейшее превращение в ходе серии реакций имидазолонпропионовой кислоты приводит к образованию аммиака, глутамата и одноуглеродного фрагмента, соединённого с тетрагидофолиевой кислотой.
Реакция декарбоксилирования гистидина имеет большое физиологическое значение, так как является источником образования биологически активного вещества — гистамина, который играет важную роль в процессе воспаления и развития некоторых аллергических реакций.
Декарбоксилирование происходит большей частью в тучных клетках соединительной ткани практически всех органов. Эта реакция протекает при участии фермента гистидиндекарбоксилазы.
Известно связанное с дефектом гистидиназы наследственное заболевание гистидинемия, при котором характерно повышенное содержание гистидина в тканях и задержка умственного и физического развития.
Биосинтез
Биосинтез гистидина не осуществляется de novo в людях и других животных, поэтому аминокислота должна употребляться в чистом виде или в составе других белков.
Примечания
| Это заготовка статьи по биохимии. Вы можете помочь проекту, дополнив её. |
Для улучшения этой статьи желательно: |
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .