| 5-HT₇-рецептор | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||||||
| Символ | HTR7 ; 5-HT₇ | ||||||||||||
| Внешние ID | OMIM: 182137 MGI: 99841 HomoloGene: 20244 IUPHAR: 5-HT7 ChEMBL: 3155 GeneCards: HTR7 Gene | ||||||||||||
| |||||||||||||
| Профиль экспрессии РНК | |||||||||||||
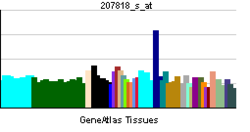 | |||||||||||||
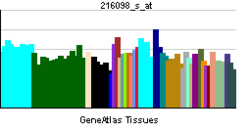 | |||||||||||||
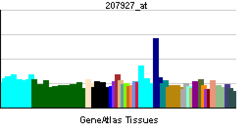 | |||||||||||||
| Больше информации | |||||||||||||
| Ортологи | |||||||||||||
| Вид | Человек | Мышь | |||||||||||
| Entrez | 3363 | 15566 | |||||||||||
| Ensembl | ENSG00000148680 | ENSMUSG00000024798 | |||||||||||
| UniProt | P34969 | P32304 | |||||||||||
| RefSeq (мРНК) | NM_000872 | NM_008315 | |||||||||||
| RefSeq (белок) | NP_000863 | NP_032341 | |||||||||||
| Локус (UCSC) | Chr 10: 92.5 – 92.62 Mb | Chr 19: 35.96 – 36.06 Mb | |||||||||||
| Поиск в PubMed | |||||||||||||
5-HT₇-рецептор — это один из подтипов серотониновых рецепторов, относящийся к семейству метаботропных G-белок-связанных рецепторов на мембране клетки. Он активируется нейромедиатором серотонином (5-гидрокситриптамином, 5-HT)[1]. Рецепторы подтипа 5-HT₇ связаны с гетеротримерным G-белком Gs, который стимулирует образование внутриклеточных сигнальных молекул (вторичных мессенджеров) — молекул цАМФ.[2][3] Он экспрессируется в различных тканях человека, в особенности в мозге, в желудочно-кишечном тракте и в кровеносных сосудах.[3] В последнее время 5-HT₇-рецептор является мишенью для разработки новых лекарств, предназначенных для лечения различных заболеваний, в частности, лекарств для лечения депрессий, то есть антидепрессантов.[4] Рецепторы подтипа 5-HT₇ кодируются геном HTR7, который у человека транскрипционируется путём альтернативного сплайсинга в 3 различных сплайс-варианта — 5-HT₇(a), 5-HT₇(b), 5-HT₇(d). Вариант 5-HT₇(c) у человека отсутствует, зато имеется у крыс, у которых отсутствует 5-HT₇(d)[5].
Функция
У человека нейромедиатор серотонин играет важную роль в регуляции различных когнитивных, эмоциональных и поведенческих функций и реакций. Многие из этих регуляторных функций, по-видимому, осуществляются именно через рецепторы подтипа 5-HT₇. Эти рецепторы, кодируемые геном HTR7, относятся к суперсемейству G-белок-связанных рецепторов. Когда 5-HT₇ рецептор активируется серотонином, запускается нисходящий сигнальный каскад, начинающийся с высвобождения из GPCR-комплекса стимулирующего гетеротримерного G-белка, так называемого Gsα. В свою очередь, этот белок Gsα активирует аденилатциклазу, что приводит к повышению внутриклеточного уровня вторичного мессенджера — циклического аденозинмонофосфата.
Рецепторы подтипа 5-HT₇ играют роль в расслаблении гладких мышц сосудов и желудочно-кишечного тракта.[1] В мозгу наиболее высокая плотность 5-HT₇-рецепторов обнаруживается в таламусе и гипоталамусе. Достаточно высокие концентрации этого рецептора обнаруживаются также в гиппокампе, лимбической системе и коре. Рецепторы подтипа 5-HT₇ вовлечены в регуляцию температуры тела, циркадного ритма, сна, процессов обучения и памяти. Существуют также данные о том, что 5-HT₇-рецепторы могут быть вовлечены в регуляцию настроения и эмоций, что, возможно, делает их важной мишенью при лечении депрессий и при разработке новых антидепрессантов.[6][7]
Открытие
В 1983 году было впервые обнаружено свидетельство существования особого подтипа серотониновых рецепторов, функционально сходного с 5-HT₁, но не идентичного ему.[8] Десять лет спустя, в 1993 году, был выделен, клонирован и охарактеризован 5-HT₇-рецептор.[3] После этого стало очевидным, что рецептор, впервые описанный в 1983 году, является именно 5-HT₇-рецептором.[9]
Варианты альтернативного сплайсинга
У человека обнаружены три варианта альтернативного сплайсинга, обозначаемые h5-HT₇(a), h5-HT₇(b) и h5-HT₇(d), которые кодируют рецепторы, отличающиеся лишь C-концом.[5] Вариант рецептора h5-HT₇(a) является вариантом полной длины (445 аминокислот),[3] в то время как вариант h5-HT₇(b) — это тот же белок, обрезанный на 432-й аминокислоте вследствие наличия альтернативного донорского сплайсинг-сайта. Изоформа h5-HT₇(d) отличается: удержание экзоновой кассеты в регионе, кодирующем C-конец белка, вызывает образование аминокислотной последовательности из 479 аминокислот с C-терминальным концом, значительно отличающимся от h5-HT₇(a). Сплайсинг-вариант 5-HT₇(c) обнаруживается в тканях крысы, но не обнаруживается у человека. И наоборот, крысы не экспрессируют вариант сплайсинга, гомологичный человеческому h5-HT₇(d), потому что крысиный ген белка 5-HT₇-рецептора не имеет экзона, необходимого для кодирования этой изоформы.[5] Аффинность различных лекарств к разным вариантам сплайсинга 5-HT₇-рецептора сходна;[10] однако эффективность обратных агонистов (степень их внутренней обратной агонистической активности), судя по всему, зависит от сплайс-варианта рецептора, то есть отличается для разных вариантов сплайсинга.[11]
Клиническое значение
Ген белка 5-HT₇-рецептора является возможным кандидатом на вовлечённость в развитие аутизма и ряда других психических заболеваний.[12]
Лиганды
С рецепторами подтипа 5-HT₇ со средней или высокой степенью аффинитета связывается значительное количество разнообразных лигандов.
Агонисты
Агонисты имитируют эффекты эндогенного лиганда, которым для 5-HT₇-рецепторов является серотонин (связывание серотонина с 5-HT₇-рецепторами приводит к повышению внутриклеточного уровня циклического АМФ).
- 5-карбоксамидотриптамин (5-CT)
- 5-метокситриптамин (5-MT, 5-MeOT)
- 8-OH-DPAT (смешанный 5-HT1A / 5-HT₇ агонист)[13]
- арипипразол (слабый парциальный агонист, однако связывается с рецептором сильнее серотонина, и, таким образом, фактически является антагонистом)[14]
- AS-19
- E-55888[15]
- E-57431[16]
- LP-12 (4-(2-дифенил)-N-(1,2,3,4-тетрагидронафтален-1-ил)-1-пиперазин-гексанамид)
- LP-44 (4-[2-(метилтио)фенил]-N-(1,2,3,4-тетрагидро-1-нафталенил)-1-пиперазин-гексанамид)
- LP-211
- ЛСД
- MSD-5a[17]
- Nω-метилсеротонин[18]
- N-(1,2,3,4-тетрагидронафтален-1-ил)-4-арил-1-пиперазин-гексанамиды (могут быть как агонистами, так и антагонистами в зависимости от того, какими радикалами замещена боковая цепь)[19][20]
- N,N-диметилтриптамин
- RA-7 (1-(2-дифенил)пиперазин)
Антагонисты
Нейтральные антагонисты (также называемые «молчаливыми антагонистами») связываются с рецепторами, но не имеют собственной внутренней активности, и лишь блокируют связывание с рецептором как агонистов, так и обратных агонистов.
Обратные агонисты ингибируют конституциональную (встроенную) активность рецептора, вызывая эффекты, противоположные эффектам агонистов (в случае 5-HT₇-рецептора — эффект снижения содержания в клетке циклического АМФ).[21][22] Обычно в литературе и нейтральные антагонисты, и обратные агонисты описываются вместе под одной рубрикой «антагонисты». В случае 5-HT₇-рецепторов проведение грани между нейтральными антагонистами и обратными агонистами осложняется ещё и тем, что внутренняя антагонистическая (то есть обратная агонистическая) активность различных лигандов-антагонистов различна по отношению к различным вариантам альтернативного сплайсинга 5-HT₇-рецептора. Так, например, месулергин и метерголин считаются нейтральными антагонистами по отношению к изоформам рецептора h5-HT₇(a) и h5-HT₇(d), но проявляют выраженную обратную агонистическую активность по отношению к h5-HT₇(b) варианту сплайсинга 5-HT₇-рецептора.
Нейтральные антагонисты
Сильными антагонистами 5-HT₇-рецепторов являются многие антидепрессанты и многие атипичные антипсихотики, а также некоторые из типичных антипсихотиков (в частности трифлуоперазин, фторфеназин). Это может, наряду с другими механизмами, частично обуславливать антидепрессивный эффект этих антидепрессантов и атипичных антипсихотиков, а также способность указанных антипсихотиков потенцировать действие антидепрессантов.
Антагонистами 5-HT₇-рецепторов являются также многие противомигренозные препараты, такие, как метисергид, кетансерин, ритансерин. Возможно, что антагонизм по отношению к 5-HT₇-рецепторам вносит свой вклад в их антимигренозное профилактическое действие.
Предположение о связи антагонизма к 5-HT₇ с наличием или усилением антидепрессивной активности служило одним из мотивов к разработке вортиоксетина — новейшего СИОЗСН, который, помимо способности к ингибированию обратного захвата серотонина и норадреналина, обладает также тропностью к целому ряду серотониновых рецепторов, в частности является сильным антагонистом 5-HT₇-рецепторов.
Антидепрессанты
- амитриптилин
- амоксапин
- кломипрамин
- имипрамин
- мапротилин
- миансерин
- вортиоксетин
Атипичные антипсихотики
- амисульприд[23]
- сульпирид
- оланзапин
- клозапин
- зипрасидон
- лурасидон
- сертиндол
- зотепин
Традиционные (типичные) антипсихотики
- фторфеназин
- трифлуоперазин
- спиперон
- локсапин
Антимигренозные препараты
- метисергид
- месулергин
- кетансерин
- ритансерин
Антидементные препараты
- флуперлапин
- тенилапин
Разное
- ципрогептадин
Исследовательские препараты
- 3-{4-[4-(4-хлорфенил)-пиперазин-1-ил]-бутил}-3-этил-6-фторо-1,3-дигидро-2H-индол-2-он[24]
- DR-4485
- EGIS-12233 (смешанный 5-HT₆- / 5-HT₇-антагонист)
- ICI 169,369
- LY-215,840
- SB-258,719[25][26][27]
- SB-258,741[27]
- SB-269,970 (высоко селективный по отношению к 5-HT₇-рецепторам)[28]
- SB-656,104-A[29]
- SB-691,673[25]
- TFMPP
Инактивирующие антагонисты
Инактивирующие антагонисты являются неконкурентными антагонистами, которые вызывают перманентную нечувствительность рецептора к агонисту (даже после освобождения рецептора от связывания с инактивирующим антагонистоv), что напоминает эффект десенситизации рецепторов, наблюдаемый при их длительной или повторяющейся стимуляции агонистом. Однако инактивация 5-HT₇-рецепторов существующими на сегодня «инактивирующими антагонистами» происходит не по классическим механизмам рецепторной инактивации или десенситизации, таким, как фосфорилирование рецепторного белка, связывание рецепторного белка с бета-арестином или интернализация рецептора (его «проваливание» внутрь клетки).[30] Вместо этого существующие на сегодняшний день инактивирующие антагонисты необратимо или псевдо-необратимо ковалентно связываются с 5-HT₇ рецептором, как показывают опыты с меченым радиоактивным [3H]-рисперидоном.[31][32]
Характерно, что среди инактивирующих антагонистов 5-HT₇-рецепторов, опять-таки, обнаруживаются уже известные антимигренозные соединения, а также уже известные типичные и атипичные антипсихотики. Возможно, что наличие у бромокриптина и лизурида антидепрессивной активности связано не только с их агонизмом к D₂-рецепторам, но и с их необратимым антагонизмом к 5-HT₇-рецепторам и ряду других серотониновых рецепторов. То же замечание касается рисперидона и палиперидона.
Антимигренозные препараты
- метерголин[32]
Дофаминергические агонисты
- бромокриптин[32]
- лизурид[32]
Типичные антипсихотики
- метиотепин[31]
Атипичные антипсихотики
Примечания
- 1 2 Vanhoenacker P, Haegeman G, Leysen JE (February 2000). “5-HT₇ receptors: current knowledge and future prospects”. Trends Pharmacol. Sci. 21 (2): 70—7. DOI:10.1016/S0165-6147(99)01432-7. PMID 10664612.
- ↑ Ruat M, Traiffort E, Leurs R, Tardivel-Lacombe J, Diaz J, Arrang JM, Schwartz JC (September 1993). “Molecular cloning, characterization, and localization of a high-affinity serotonin receptor (5-HT₇) activating cAMP formation”. Proc. Natl. Acad. Sci. U.S.A. 90 (18): 8547—51. DOI:10.1073/pnas.90.18.8547. PMC 47394. PMID 8397408.
- 1 2 3 4 Bard JA, Zgombick J, Adham N, Vaysse P, Branchek TA, Weinshank RL (November 1993). “Cloning of a novel human serotonin receptor (5-HT₇) positively linked to adenylate cyclase”. J. Biol. Chem. 268 (31): 23422—6. PMID 8226867.
- ↑ Mnie-Filali O, Lambás-Señas L, Zimmer L, Haddjeri N (December 2007). “5-HT₇ receptor antagonists as a new class of antidepressants”. Drug News Perspect. 20 (10): 613—8. DOI:10.1358/dnp.2007.20.10.1181354. PMID 18301795.
- 1 2 3 Heidmann DE, Metcalf MA, Kohen R, Hamblin MW (April 1997). “Four 5-hydroxytryptamine7 (5-HT₇) receptor isoforms in human and rat produced by alternative splicing: species differences due to altered intron-exon organization”. J. Neurochem. 68 (4): 1372—81. DOI:10.1046/j.1471-4159.1997.68041372.x. PMID 9084407.
- ↑ Hedlund PB, Sutcliffe JG (September 2004). “Functional, molecular and pharmacological advances in 5-HT₇ receptor research”. Trends Pharmacol. Sci. 25 (9): 481—6. DOI:10.1016/j.tips.2004.07.002. PMID 15559250.
- ↑ Naumenko VS, Popova NK, Lacivita E, Leopoldo M, Ponimaskin EG (2014). “Interplay between Serotonin 5-HT1A and 5-HT₇ Receptors in Depressive Disorders”. CNS Neurosci Ther. 20 (7): 582—90. DOI:10.1111/cns.12247. PMID 24935787.
- ↑ Feniuk W., Humphrey P. P., Watts A. D. 5-Hydroxytryptamine-induced relaxation of isolated mammalian smooth muscle. (англ.) // European journal of pharmacology. — 1983. — Vol. 96, no. 1-2. — P. 71—78. — PMID 6662198.
- ↑ Hoyer D., Hannon J. P., Martin G. R. Molecular, pharmacological and functional diversity of 5-HT receptors. (англ.) // Pharmacology, biochemistry, and behavior. — 2002. — Vol. 71, no. 4. — P. 533—554. — PMID 11888546.
- ↑ Krobert KA, Bach T, Syversveen T, Kvingedal AM and Levy FO (2001) The cloned human 5-HT7 receptor splice variants: a comparative characterization of their pharmacology, function and distribution. Naunyn Schmiedebergs Arch Pharmacol 363(6):620-632. (2001). “The cloned human 5-HT7 receptor splice variants: a comparative characterization of their pharmacology, function and distribution”. Naunyn-Schmiedeberg's archives of pharmacology. 363 (6): 620—32. DOI:10.1007/s002100000369. PMID 11414657.
- ↑ Krobert KA and Levy FO (2002) The human 5-HT7 serotonin receptor splice variants: constitutive activity and inverse agonist effects. Br J Pharmacol 135(6):1563-1571. (2002). “The human 5-HT7 serotonin receptor splice variants: constitutive activity and inverse agonist effects”. British Journal of Pharmacology. 135 (6): 1563—71. DOI:10.1038/sj.bjp.0704588. PMC 1573253. PMID 11906971.
- ↑ Lassig JP, Vachirasomtoon K, Hartzell K, Leventhal M, Courchesne E, Courchesne R, Lord C, Leventhal BL, Cook EH (October 1999). “Physical mapping of the serotonin 5-HT₇ receptor gene (HTR7) to chromosome 10 and pseudogene (HTR7P) to chromosome 12, and testing of linkage disequilibrium between HTR7 and autistic disorder”. Am. J. Med. Genet. 88 (5): 472—5. DOI:10.1002/(SICI)1096-8628(19991015)88:5<472::AID-AJMG7>3.0.CO;2-G. PMID 10490701.
- ↑ Sprouse J, Reynolds L, Li X, Braselton J, Schmidt A (2004). “8-OH-DPAT as a 5-HT₇ agonist: phase shifts of the circadian biological clock through increases in cAMP production”. Neuropharmacology. 46 (1): 52—62. DOI:10.1016/j.neuropharm.2003.08.007. PMID 14654097.
- ↑ Davies MA, Sheffler DJ, Roth BL. Aripiprazole: A Novel Atypical Antipsychotic Drug With a Uniquely Robust Pharmacology. CNS Drug Reviews [Internet]. 2004 [cited 2013 Aug 4];10(4):317-36. Available from: http://onlinelibrary.wiley.com/doi/10.1111/j.1527-3458.2004.tb00030.x/pdf
- ↑ Brenchat A, Ejarque M, Zamanillo D, Vela JM, Romero L (August 2011). “Potentiation of Morphine Analgesia by Adjuvant Activation of 5-HT₇ Receptors”. Journal of Pharmacological Sciences. 116 (4): 388—91. DOI:10.1254/jphs.11039sc. PMID 21778664.
- ↑ Brenchat A, Nadal X, Romero L, Ovalle S, Muro A, Sánchez-Arroyos R, Portillo-Salido E, Pujol M, Montero A, Codony X, Burgueño J, Zamanillo D, Hamon M, Maldonado R, Vela JM (June 2010). “Pharmacological activation of 5-HT₇ receptors reduces nerve injury-induced mechanical and thermal hypersensitivity”. Pain. 149 (3): 483—94. DOI:10.1016/j.pain.2010.03.007. PMID 20399562.
- ↑ Brenchat A, Romero L, García M, Pujol M, Burgueño J, Torrens A, Hamon M, Baeyens JM, Buschmann H, Zamanillo D, Vela JM (February 2009). “5-HT₇ receptor activation inhibits mechanical hypersensitivity secondary to capsaicin sensitization in mice”. Pain. 141 (3): 239—47. DOI:10.1016/j.pain.2008.11.009. PMID 19118950.
- ↑ Powell SL, Gödecke T, Nikolic D, Chen SN, Ahn S, Dietz B, Farnsworth NR, van Breemen RB, Lankin DC, Pauli GF, Bolton JL (2008). “In vitro serotonergic activity of black cohosh and identification of N(omega)-methylserotonin as a potential active constituent”. J Agric Food Chem. 56 (24): 1718—1726. DOI:10.1021/jf803298z. PMID 19049296.
- ↑ Leopoldo M, Lacivita E, Contino M, Colabufo NA, Berardi F, Perrone R (2007). “Structure-activity relationship study on N-(1,2,3,4-tetrahydronaphthalen-1-yl)-4-aryl-1-piperazinehexanamides, a class of 5-HT7 receptor agents. 2”. J. Med. Chem. 50 (17): 4214—21. DOI:10.1021/jm070487n. PMID 17649988.
- ↑ Leopoldo M, Berardi F, Colabufo NA; et al. (2004). “Structure-affinity relationship study on N-(1,2,3,4-tetrahydronaphthalen-1-yl)-4-aryl-1-piperazinealkylamides, a new class of 5-hydroxytryptamine7 receptor agents”. J. Med. Chem. 47 (26): 6616—24. DOI:10.1021/jm049702f. PMID 15588097.
- ↑ Pittalà V, Salerno L, Modica M, Siracusa MA, Romeo G (2007). “5-HT₇ receptor ligands: recent developments and potential therapeutic applications”. Mini Rev Med Chem. 7 (9): 945—60. DOI:10.2174/138955707781662663. PMID 17897083.
- ↑ Leopoldo M (2004). “Serotonin(7) receptors (5-HT7Rs) and their ligands”. Curr. Med. Chem. 11 (5): 629—61. DOI:10.2174/0929867043455828. PMID 15032609.
- ↑ Abbas AI, Hedlund PB, Huang XP, Tran TB, Meltzer HY, Roth BL (July 2009). “Amisulpride is a potent 5-HT₇ antagonist: relevance for antidepressant actions in vivo”. Psychopharmacology (Berl.). 205 (1): 119—28. DOI:10.1007/s00213-009-1521-8. PMC 2821721. PMID 19337725.
- ↑ Volk B, Barkóczy J, Hegedus E; et al. (April 2008). “(Phenylpiperazinyl-butyl)oxindoles as selective 5-HT₇ receptor antagonists”. J. Med. Chem. 51 (8): 2522—32. DOI:10.1021/jm070279v. PMID 18361484.
- 1 2 Romero G, Pujol M, Pauwels PJ (2006). “Reanalysis of constitutively active rat and human 5-HT₇(a) receptors in HEK-293F cells demonstrates lack of silent properties for reported neutral antagonists”. Naunyn Schmiedebergs Arch. Pharmacol. 374 (1): 31—9. DOI:10.1007/s00210-006-0093-y. PMID 16967291.
- ↑ Forbes IT, Dabbs S, Duckworth DM; et al. (February 1998). “(R)-3,N-dimethyl-N-[1-methyl-3-(4-methyl-piperidin-1-yl) propyl]benzenesulfonamide: the first selective 5-HT₇ receptor antagonist”. J. Med. Chem. 41 (5): 655—7. DOI:10.1021/jm970519e. PMID 9513592.
- 1 2 Mahé C, Loetscher E, Feuerbach D, Müller W, Seiler MP, Schoeffter P (2004). “Differential inverse agonist efficacies of SB-258719, SB-258741 and SB-269970 at human recombinant serotonin 5-HT7 receptors”. Eur. J. Pharmacol. 495 (2–3): 97—102. DOI:10.1016/j.ejphar.2004.05.033. PMID 15249157.
- ↑ Lovell PJ, Bromidge SM, Dabbs S, Duckworth DM, Forbes IT, Jennings AJ, King FD, Middlemiss DN, Rahman SK, Saunders DV, Collin LL, Hagan JJ, Riley GJ and Thomas DR (2000) A novel, potent, and selective 5-HT₇ antagonist: (R)-3-(2-(2-(4-methylpiperidin-1-yl)ethyl)pyrrolidine-1-sulfonyl) phen ol (SB-269970). J Med Chem 43(3):342-345. (2000). “A novel, potent, and selective 5-HT₇ antagonist: (R)-3-(2-(2-(4-methylpiperidin-1-yl)ethyl)pyrrolidine-1-sulfonyl) phen ol (SB-269970)”. Journal of Medical Chemistry. 43 (3): 342—5. DOI:10.1021/jm991151j. PMID 10669560.
- ↑ Forbes IT, Douglas S, Gribble AD; et al. (November 2002). “SB-656104-A: a novel 5-HT₇ receptor antagonist with improved in vivo properties”. Bioorg. Med. Chem. Lett. 12 (22): 3341—4. DOI:10.1016/S0960-894X(02)00690-X. PMID 12392747.
- ↑ Zhang J, Ferguson SS, Barak LS, Aber MJ, Giros B, Lefkowitz RJ and Caron MG (1997) Molecular mechanisms of G protein-coupled receptor signaling: role of G protein-coupled receptor kinases and arrestins in receptor desensitization and resensitization. Receptors Channels 5(3-4):193-199. (1997). “Molecular mechanisms of G protein-coupled receptor signaling: role of G protein-coupled receptor kinases and arrestins in receptor desensitization and resensitization”. Receptors & channels. 5 (3–4): 193—9. PMID 9606723.
- 1 2 3 4 Smith C, Rahman T, Toohey N, Mazurkiewicz J, Herrick-Davis K and Teitler M (2006) Risperidone irreversibly binds to and inactivates the h5-HT₇ serotonin receptor. Mol Pharmacol 70(4):1264-1270. (2006). “Risperidone irreversibly binds to and inactivates the h5-HT7 serotonin receptor”. Molecular Pharmacology. 70 (4): 1264—70. DOI:10.1124/mol.106.024612. PMID 16870886.
- 1 2 3 4 Knight JA, Smith C, Toohey N, Klein MT and Teitler M (2009) Pharmacological analysis of the novel, rapid, and potent inactivation of the human 5-Hydroxytryptamine7 receptor by risperidone, 9-OH-Risperidone, and other inactivating antagonists. Mol Pharmacol 75(2):374-380. (2009). “Pharmacological analysis of the novel, rapid, and potent inactivation of the human 5-Hydroxytryptamine7 receptor by risperidone, 9-OH-Risperidone, and other inactivating antagonists”. Molecular Pharmacology. 75 (2): 374—80. DOI:10.1124/mol.108.052084. PMC 2671286. PMID 18996971.
Ссылки
- 5-HT7. IUPHAR Database of Receptors and Ion Channels. International Union of Basic and Clinical Pharmacology.
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .