| N-Диметилформамид N | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
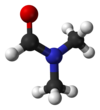
N,N-Диметилформамид |
| Сокращения | DMF, ДМФА |
| Хим. формула | C3H7NO |
| Рац. формула | (CH3)2NC(O)H |
| Физические свойства | |
| Состояние | прозрачная жидкость |
| Молярная масса | 73.09 г/моль |
| Плотность | 0,9445 г/см³ |
| Динамическая вязкость | 0,92 мПа·с (20 °C) |
| Энергия ионизации | 9,12 ± 0,01 эВ[1] |
| Термические свойства | |
| Т. плав. | -61 °C |
| Т. кип. | 153 °C |
| Т. всп. | 59 °C |
| Пр. взрв. | 2,2 ± 0,1 об.%[1] |
| Мол. теплоёмк. | 148,37 Дж/(моль·К) |
| Энтальпия образования | 192 кДж/моль |
| Удельная теплота испарения | 42,3 Дж/кг |
| Давление пара | 3 ± 1 мм рт.ст.[1] |
| Химические свойства | |
| Растворимость в воде | ∞ |
| Растворимость в в спирте | ∞ |
| Оптические свойства | |
| Показатель преломления | 1,43 |
| Структура | |
| Дипольный момент | 3,82 Д |
| Классификация | |
| Рег. номер CAS | 68-12-2 |
| PubChem | 6228 |
| Рег. номер EINECS | 200-679-5 |
| SMILES | |
| InChI | |
| RTECS | LQ2100000 |
| ChEBI | 17741 и 42077 |
| Номер ООН | 2265 |
| ChemSpider | 5993 |
| Безопасность | |
| ЛД50 | 4,2 мг/кг (мыши, перорально) |
| NFPA 704 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
N,N-Диметилформамид (Диметилформамид, сокр. ДМФА) — органическое соединение с формулой (CH3)2NC(O)H. Бесцветная довольно вязкая жидкость со слабым специфическим «рыбным» запахом из-за наличия продукта разложения — диметиламина. В чистом виде практически без запаха.
Структура и свойства
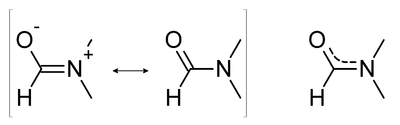
Благодаря наличию двух резонансных форм в диметилформамиде порядок связи С=O уменьшен, а С-N увеличен. Так в инфракрасном спектре наблюдается понижение частоты карбонильной группы (1675 см−1) по сравнению с таковой для свободной. Также благодаря частично двойному характеру связи азот-углерод, при комнатной температуре заторможено вращение вокруг неё в шкале времени ПМР. При этом наблюдается два сигнала (синглеты) метильной группы интенсивностью 3 протона δ 2.97 и 2.88, вместо одного синглета 6 протонов.
ДМФА смешивается с большинством органических растворителей за исключением углеводородов. Часто используемый растворитель для проведения химических реакций и очистки веществ перекристаллизацией, благодаря высокой растворяющей способности как для органических соединений так и частично для неорганических солей. ДМФА является полярным апротонным растворителем с высокой точкой кипения. Он способствует прохождению реакций с полярным механизмом, таких как SN2 реакций. Неустойчив к действию сильных кислот и оснований, что приводит к гидролизу, особенно при высоких температурах. Диэлектрическая проницаемость равна 36,71.
Получение
- по реакции между диметиламином и угарным газом в метаноле (100—150 °C, 2,5-20 МПа) в присутствии CH3ONa или карбонилов металлов:
- реакцией метилформиата с диметиламином (80-120 °C и 0,1-0,4 МПа):
- реакцией муравьиной кислоты с диметиламином:
Очистка
Диметилформамид-сырец, содержащий незначительные количества влаги, диметиламина, формиата диметиламмония и монометилформамида, очищают вакуумной ректификацией. Примеси воды и муравьиной кислоты удаляются также перемешиванием или встряхиванием с гидроксидом калия и последующей перегонкой над BaO или CaO.
Применение
- как растворитель при производстве полиакрилонитрильного волокна (нитрона), и других полимеров
- для растворения красителей при крашении кожи, бумаги, древесины, вискозы и др.
- для абсорбции HCl, SO2 и других кислотных газов
- наряду с ацетонитрилом, является часто употребляемым растворителем в спектроскопии ЭПР
- как растворитель при реставрации художественных произведений изобразительного искусства, как выполненных в технике темперной, так и масляной живописи.
- для получения альдегидов по Вильсмаеру:

и Буво:

- для проведения спектроскопических исследований в ближней инфракрасной области
- в кислотно-основном титровании слабых кислот в неводных средах (в качестве среды)
- в составе ИПП-8 для оказания первой помощи при поражении капельножидкими отравляющими веществами
Безопасность
Реакция с использованием гидрида натрия в ДМФА отчасти опасна. Сообщалось об экзотермическом разложении выше 26 °C. В лабораторных условиях данная проблема решается использованием бань со льдом. В опытных производствах сообщалось о нескольких инцидентах при использовании данных реагентов.
Токсичность
Обладает довольно сильным раздражающим действием на слизистые оболочки и кожные покровы. Проникая в организм, проявляет резорбтивное действие: повреждает печень и почки. Центральную нервную систему угнетает слабо. Отравления возможны в результате приёма вещества внутрь и его всасывания с поверхности кожи. Примерная смертельная доза 10 г. ДМФА раздражает кожу и слизистые оболочки, проникает через неповреждённую кожу, проявляет общетоксическое и эмбриотоксическое воздействие на организм. Вызывает поражение печени, почек, сердца.
Предполагается, что ДМФА является канцерогеном, также ему приписывают появление врождённых патологий. Для проведения многих реакций он может быть заменён диметилсульфоксидом. Раздражает слизистые оболочки глаз. ПДК в воздухе рабочей зоны N,N-диметилформамида — 10 мг/м³.
Примечания
Литература
- Якушкин М. И., Котов В. И. Справочник нефтехимика / Под ред. С. К. Огородникова. — Л., 1978. — Т. 2. — С. 295—297.
- Гордон А., Форд Р. Спутник химика / Пер. с англ. Розенберга Е. Л., Коппель С. И.. — М.: Мир, 1976. — 544 с.
- Новый справочник химика и технолога. Радиоактивные вещества. Вредные вещества. Гигиенические нормативы / Редкол.: Москвин А. В. и др.. — СПб.: АНО НПО «Профессионал», 2004. — 1142 с.
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .




