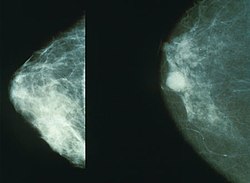
| Рак молочной железы | |
|---|---|
 | |
| МКБ-10 | C50. |
| МКБ-9 | 174-175 |
| OMIM | 114480 |
| DiseasesDB | 1598 |
| MedlinePlus | 000913 |
| eMedicine | med/2808 |
| MeSH | D001943 |
Рак моло́чной железы́ — злокачественная опухоль железистой ткани молочной железы. В мире это наиболее частая форма рака среди женщин, поражающая в течение жизни от 1/13 до 1/9 женщин в возрасте от 13 до 90 лет. Это также второе по частоте после рака лёгких онкологическое заболевание в популяции в целом (считая и мужское население; поскольку молочная железа состоит из одинаковых тканей у мужчин и женщин, рак молочной железы (РМЖ) иногда встречается и у мужчин, но случаи этого вида рака у мужчин составляют менее 1 % от общего количества больных данным заболеванием).
По оценкам экспертов ВОЗ, в мире ежегодно регистрируют от 800 тыс. до 1 млн новых случаев заболевания раком молочной железы[1]. По числу смертей от рака у женщин эта разновидность рака занимает второе место. Наиболее высока заболеваемость в США и Западной Европе; в России в 2005 году было выявлено 49 548 новых случаев заболевания (19,8 % всех видов опухолей у женщин), а число умерших составило 22 830[2]. В 2010 году рак молочной железы занимал 1-е место как в структуре заболеваемости женского населения России злокачественными новообразованиями (20,5 %), так и в структуре смертности от таких заболеваний (17,2 %); при этом число впервые выявленных случаев рака молочной железы выросло до 57 241[1].
За резкое увеличение количества случаев рака молочной железы в развитых странах после 1970-х годов считают частично ответственным изменившийся стиль жизни населения этих стран (в частности то, что в семьях стало меньше детей и сроки грудного вскармливания сократились)[3]. Во многом наблюдающееся в последнее время в развитых странах возрастание числа онкологических больных связано также с обогащением популяции всё более пожилыми людьми. При этом риск развития рака молочной железы в возрасте после 65 лет в 5,8 раз выше, чем до 65 лет, и почти в 150 раз выше, чем в возрасте до 30 лет[4].
Рак молочной железы — многофакторное заболевание, развитие которого связано с изменением генома клетки под воздействием внешних причин и гормонов[5].
Исторические описания

Рак молочной железы является одной из самых изученных и изучаемых форм рака. Древнейшее из известных описаний рака молочной железы (хотя сам термин «рак» ещё не был известен и не использовался) было найдено в Египте и датируется примерно 1600 годом до н. э. Так называемый «Папирус Эдвина Смита» описывает 8 случаев опухолей или изъязвлений молочной железы, которые были подвергнуты лечению прижиганием огнём. Текст гласит: «От этой болезни нет лечения; она всегда приводит к смерти».
В течение многих столетий врачи описывали подобные случаи в своей практике с тем же печальным заключением. Никаких сдвигов в лечении рака молочной железы не происходило до тех пор, пока в XVII веке врачи не добились лучшего понимания работы кровеносной и лимфатической систем организма и не смогли понять, что рак молочной железы распространяется (метастазирует) по лимфатическим путям и в первую очередь поражает ближайшие — подмышечные — лимфатические узлы. Французский хирург Жан-Луи Пети (1674—1750) и вскоре после него шотландский хирург Бенджамин Белл[en] (1749—1806) были первыми, кто догадался удалять при раке молочной железы не только саму молочную железу, но и ближайшие лимфатические узлы и подлежащую грудную мышцу. Их успешная работа была подхвачена Уильямом Стюартом Холстедом (1852—1922), который в 1882 году ввёл в широкую медицинскую практику технически усовершенствованный вариант этой операции, которую он назвал «радикальной мастэктомией». Операция стала настолько популярной при раке молочной железы, что даже получила название по имени её изобретателя — «мастэктомия Холстеда» или «мастэктомия по Холстеду».
Этиология и факторы риска
Вопросы этиологии рака молочной железы в настоящее время исследованы недостаточно. В отличие от рака лёгкого или рака мочевого пузыря, ни один из канцерогенов окружающей среды не удаётся убедительно связать с провокацией рака молочной железы[4]. Согласно исследованию учёных из Университета Тафтса, риск развития рака молочной железы повышает бисфенол А (BPA), содержащийся в пищевом пластике. [6].
В ряде случаев рак молочной железы предстаёт как классическое наследственное заболевание. Наиболее выраженными генетическими факторами предрасположенности к раку молочной железы исследователи считают гены BRCA1[en]* (№ NM_007294 в базе данных GenBank) и BRCA2[en] (№ NM_007294 в GenBank); вклад наследственных мутаций в этих генах в частоту наследственный заболеваний раком молочной железы — около 20 %. Подобную роль играют и гены ATM, TP53 (ген белка p53), PTEN[7].
В настоящее время исследована экспрессия различных генов в опухолях молочной железы и выделены различные молекулярные типы опухоли. Клинически, они имеют существенно различный риск развития метастазов и требуют различной терапии. Коллекция данных[8] по экспрессии 17 816 генов в опухолях молочной железы доступна онлайн[9] и используется не только для медико-биологических исследований, но и как ставший классическим тестовый пример для визуализации и картографии данных.
Основные факторы риска
Факторы риска развития рака молочной железы[10]:
- отсутствие в анамнезе беременностей и родов;
- курение (особенно, если оно начато в юном возрасте);
- раннее менархе (до 12 лет);
- поздняя менопауза (после 55 лет);
- отягощенный семейный анамнез (онкозаболевания у кровных родственников);
- больные, леченные по поводу рака женских половых органов;
- ожирение[11];
- сахарный диабет;
- гипертоническая болезнь;
- злоупотребление алкоголем;
- употребление экзогенных гормонов — при непрерывном употреблении экзогенных гормонов с целью контрацепции или лечения — более 10 лет.
По результатам недавних исследований Калифорнийского университета в Беркли (University of California-Berkeley) 239 женщин, удалось выявить дополнительный фактор риска рака молочной железы, которым оказался вирус лейкоза коров (BLV). Исследователями допускается, что наличие в организме человека этого вируса связано с риском рака молочной железы больше, чем традиционные факторы риска: ожирение, употребление алкоголя и прием гормональных препаратов в постменопаузе. На данный момент доказана лишь связь между раком молочной железы и присутствием BLV в организме. Является ли вирус причиной развития опухоли, неизвестно.[12][13]
В исследованиях Института медицинских исследований Гарвана в Австралии обнаружено, что развитию метастазов опухоли молочной железы и прогрессированию рака способствует белок ELF5.[14]
Симптомы рака молочной железы на ранних стадиях заболевания могут отсутствовать или характеризоваться появлением в молочной железе небольших малочувствительных подвижных масс. Рост опухоли сопровождается нарушением её подвижности, фиксацией, розоватыми или оранжевыми выделениями из соска.
Классификация TNM
Т — первичная опухоль
- ТХ — первичная опухоль недоступна оценке;
- Т0 — нет признаков первичной опухоли;
- Tis — рак in situ:
- Тis (DCIS) — протоковая карцинома in situ;
- Тis (LCIS) — дольковая карцинома in situ;
- Тis (Paget) — болезнь Педжета соска, не связанная с инвазивной карциномой в подлежащей паренхиме молочной.
- Т1 — опухоль до 2 см.
- Т2 — опухоль от 2 см до 5 см.
- Т3 — опухоль более 5 см;
- Т4 — опухоль любого размера с распространением на грудную стенку, кожу (изъязвление или узелки на коже)
N — регионарные лимфатические узлы
- NХ — регионарные лимфатические узлы не могут быть оценены.
- N0 — нет метастаз в регионарных лимфатических узлах;
- N1 — метастазы в подмышечных лимфатических узлах I, II уровня не спаянные между собой
- N2 -а) метастазы в подмышечных лимфатических узлах I, II уровня спаянные между собой; b) клинически определяемый внутренний маммарный лимфатический узел при отсутствии клинических признаков метастазов в подмышечных лимфатических узлах;
- N3 — а) метастазы в подключичных лимфатических узлах III уровня; b) метастазы во внутренних маммарных и подмышечных лимфатических узлах; метастазы в надключичных лимфатических узлах.
М — отдаленные метастазы
- М0 — отдаленные метастазы не определяются;
- М1 — имеются отдаленные метастазы.
Гистологические типы РМЖ
В гистологическом плане среди раковых опухолей молочной железы выделяют следующие типы[15]:
- Внутрипротоковый рак in situ
- Дольковый рак in situ
- Инвазивный протоковый рак
- Инвазивный дольковый рак
- Рак молочной железы с признаками воспаления
- Тубулярная карцинома
- Медуллярный рак
- Коллоидный рак (слизистый рак, перстневидно-клеточный рак)
- Папиллярный рак
- Метапластический рак (плоскоклеточный рак)
- Рак с остеокластоподобными клетками
- Аденоид-кистозный рак
- Секреторная карцинома (ювенильный рак)
- Кистозная гипертсекреторная карцинома
- Апокринный рак
- Рак с признаками эндокринного новообразования (первичная карциноидная опухоль, апудома)
- Криброзный рак
Молекулярная таксономия РМЖ
В последние годы развивается молекулярная таксономия рака молочной железы, позволившая выделить в рамках данного заболевания четыре основных молекулярных подтипа. Эти подтипы отличаются друг от друга характерными наборами молекулярных маркеров и фактически представляют собой разные болезни — с различной этиологией, молекулярным патогенезом и прогнозом, требующие специфических терапевтических подходов. Указанные подтипы опухолей различаются, во-первых, тем, какие цитокератины в них экспрессируются (базальные или люминальные), а во-вторых — наличием или отсутствием амплификации гена HER2. Приведём перечень этих подтипов (указывая в скобках частоту, с которой они встречаются)[16]:
- Люминальный подтип A (30—45 %): эстроген-зависимые малоагрессивные опухоли, избытка экспрессии рецепторов белка HER2 нет, наилучший прогноз;
- Люминальный подтип B (14—18 %): эстроген-зависимые агрессивные опухоли, выражена амплификация онкогена HER2, значительно худший прогноз;
- HER2-позитивный подтип (8—15 %): эстроген-независимые агрессивные опухоли, выражена амплификация онкогена HER2, повышенная вероятность негативного исхода заболевания;
- «Triple negative» подтип (27—39 %): эстроген-независимые агрессивные опухоли, избытка экспрессии рецепторов белка HER2 нет, наихудшие показатели выживаемости.
Симптомы
Рак молочной железы на ранних стадиях (1-й и 2-й) протекает бессимптомно и не причиняет боли. Могут иметь место очень болезненные месячные, боли в молочных железах при мастопатии. Обычно рак молочной железы обнаруживают до явного появления непосредственных симптомов опухоли — либо на маммографии, либо женщина чувствует появление уплотнения в груди. Любое новообразование необходимо пунктировать для выявления раковых клеток. Наиболее точная диагностика происходит по результатам трепан-биопсии под контролем УЗИ. Много случаев диагностики болезни лишь на 3-й и 4-й стадиях, когда опухоль уже видна невооружённым глазом, имеет вид язвы или большой шишки. Может появиться не исчезающее в течение менструального цикла уплотнение в подмышечной ямке или над ключицей: эти симптомы свидетельствуют о поражении лимфоузлов, то есть метастазах в лимфоузлы, явно выражающихся уже на поздних стадиях. Болевой синдром связан с прорастанием опухоли в грудную стенку.
Прочие симптомы поздних (III—IV) стадий :
- Прозрачные или кровянистые выделения из груди
- Втяжение соска в связи с прорастанием опухоли в кожу
- Изменение цвета или структуры кожи груди в связи с прорастанием опухоли в кожу.
Диагностика
Регулярное посещение врача-маммолога — специалиста в области заболеваний молочных желез (не реже одного раза в 1—2 года). Всем женщинам старше 20 лет ранее рекомендовалось ежемесячно проводить самостоятельное обследование молочной железы. Женщинам старше 40—50 лет необходимо каждые 1—2 года (даже при отсутствии жалоб) проводить маммографические обследования[17][18].
Женщинам любого возраста с выявленными заболеваниями молочных желёз показана маммография с целью дифференциальной диагностики с использованием ультразвуковых, патоморфологических методик, в том числе интервенционной радиологии.
Самостоятельное обследование молочных желёз
Согласно мета-анализу, опубликованному в Cochrane Collaboration, два больших исследования, проведённые в России и Китае, не выявили положительного эффекта при самостоятельном обследовании молочных желез с целью ранней диагностики рака молочной железы. Результаты исследований указали на возможность повышенного риска в связи с увеличением количества биопсий молочной железы[19].
Сигналы тревоги
Сигналы тревоги рака молочной железы:
- наличие уплотнений или опухолевидных образований в одной или обеих молочных железах;
- выделения из соска любого характера, не связанные с беременностью или лактацией;
- эрозии, корочки, чешуйки, изъязвления в области соска, ареолы;
- беспричинно возникающая деформация, отек, увеличение или уменьшение размеров молочной железы;
- увеличение подмышечных или надключичных лимфоузлов.
Выявление врачом хотя бы одного из указанных «сигналов тревоги» требует срочного (в молодом возрасте от 1-й до 4-й стадии может пройти всего несколько месяцев) направления больной к онкологу-маммологу терапевтом или маммологом в онкологический диспансер, где должны быть проведены УЗИ и пункция. Затем по результатам назначается либо операция с последующей химиотерапией, либо сначала химиотерапия с последующей операцией. Велик процент невнимательного (или задерживающего) отношения медицинского персонала на районном уровне к новообразованиям, в результате чего злокачественная опухоль диагностируется на поздних (3-4 стадиях). От времени обращения до дня УЗИ может пройти месяц, а это недопустимо. Не стоит полагаться на то, что опухоль может быть доброкачественной. Быстрое обследование в медицинском учреждении поможет сохранить жизнь. Скрининг рака молочной железы проводится при физикальном обследовании молочной железы врачом любой специальности ежегодно, а также ежемесячного самообследования молочных желез. Маммография проводится женщинам от 35 до 50 лет раз в 2 года (при отягощённом личном и семейном анамнезе — 1 раз в год), женщинам после 50 лет — ежегодно. Профилактика рака молочной железы заключается в устранении факторов, способствующих его развитию, а также в оптимальной диспансеризации женщин с гиперпластическими процессами и своевременном адекватном их лечении, включая оперативные методы. Диагностика данного заболевания должна быть комплексная. Методами исследования являются: УЗИ молочных желез, пункция новообразования и трепан-биопсия под контролем УЗИ, МРТ, маммография, термомаммография - устаревший метод. Велика роль анализа крови на онкомаркер. Для установления типа опухоли делают гистологическое исследование тканей.
Дифференциальная диагностика
1.Дисгормональные заболевания
- Мастодиния (основные отличия: выраженный болевой синдром, невроз, связь с предменструальным периодом, чаще поражаются обе молочные железы у нерожавших).
- Мастопатия
- Гинекомастия
2. Доброкачественные опухоли
- Фиброаденома
- Липома
- Внутрипротоковая папиллома (наблюдаются кровянистые или обильные серозные выделения из одного протока)
3. Острый гнойный мастит
Принципы лечения
Методы лечения рака молочной железы включают в себя хирургическое лечение, лучевую терапию, а также лекарственное лечение: гормонотерапию, химиотерапию и таргетную терапию.
Лекарственное лечение рака молочной железы подразделяется на неоадъюватное и адъювантное. Неоадъюватное лечение проводится до хирургической операции для уменьшения опухоли при первично не операбельном инвазивном раке молочной железы, а адъювантное — после хирургического лечения с целью снижения риска рецидива и смерти.
- Хирургическое лечение остаётся ведущим методом лечения рака молочной железы (остальные методы лечения, как правило, применимы при локализованном процессе). В большинстве случаев выполняется мастэктомия — хирургическое удаление всей молочной железы (весьма часто — наряду с окружающими тканями); профилактическая мастэктомия показана пациенткам, у которых диагностированы мутации в BRCA1 и BRCA2[20]. В последнее время при малом размере опухоли применяют также лампэктомию, когда удаляется только опухоль; однако такая операция остаётся травматичной, ведёт к деформации молочной железы, а её применимость ограничивается рядом жёстких требований. Данных недостатков лишён недавно разработанный метод криомаммотомии, при котором через небольшой надрез кожи к опухоли подводят криозонд с температурой наконечника минус 100—120 °C; при этом опухоль замораживается и превращается в примёрзший к криозонду «ледяной шарик», который удаляется из надреза вместе с криозондом[21][22].
- Гормонотерапия рака молочной железы показана при наличии рецепторов к эстрогенам и/или прогестерону, проводится антиэстрогеном Тамоксифен, ингибиторами ароматазы (Эксеместан, Анастрозол, Летрозол), аналогами гонадотропин-рилизинг гормона (Гозерелин, Бусерелин, Лейпрорелин). Минимальная длительность гормонотерапии — 5 лет, а при наличии хотя бы одного фактора неблагоприятного прогноза — 10 лет[23]. У женщин в постменопаузе ингибиторы ароматазы оказались более эффективны, чем Тамоксифен: реже возникал рецидив (примерно на 30 %), отмечалась более низкая смертность (примерно на 15 %)[24]. Летрозол по сравнению с анастрозолом более существенно уменьшает уровни эстрадиола и эстрона сульфата[25], содержание которых значительно выше у пациенток с ожирением, чем у больных с нормальной массой тела[26] (эти данные нужно учитывать при выборе препарата для пациенток с высоким значением индекса массы тела).
- Лучевая терапия обычно применяется как дополнение (адъювантная терапия) к хирургическому лечению и осуществляется после проведения мастэктомии или лампэктомии с целью уничтожения раковых клеток, которые могут остаться на месте удалённой опухоли, и снизить риск рецидива заболевания.
- Химиотерапия нацелена на подавление клеток опухоли химическими препаратами, к которым эти клетки особенно чувствительны. Может применяться до, после и вместо хирургического лечения (когда отсутствуют показания к хирургическому вмешательству).
- Таргетная терапия применяется по отношению к пациентам, у которых опухоль экспрессирует специфический ген HER2. Для такой терапии применяют трастузумаб[en] — препарат моноклональных антител, способный блокировать активность гена HER2 в клетках опухоли молочной железы, замедляя рост данной опухоли. Обычно применяют либо в комбинации с химиотерапией, либо в виде адъювантной терапии после хирургического лечения рака молочной железы[27][28]. В последние годы для таргетной терапии HER2-позитивного рака молочной железы применяют также препараты лапатиниб, пертузумаб[en], нератиниб[en][29]. Для терапии ER- и HER2 — позитивного рака существует группа препаратов, известных как блокаторы ферментного пути CDK 4/6. При тройном негативном раке молочной железы ингибиторы CDK 4/6[30] не в состоянии заморозить рост опухоли, но могут предотвратить метастазирование раковых клеток в другие части тела, воздействуя на особый SNAIL-белок, который способствует метастазированию рака.
Адъювантная терапия бифосфонатами
Метастазы гормонзависимого рака молочной железы чаще всего выявляют в костях[31], в том числе в позвонках (следствием чего может стать их разрушение с повреждением спинного мозга). Поэтому пациенткам в менопаузе с гормон рецептор-позитивным раком молочной железы следует рассмотреть назначение бифосфонатов для уменьшения вероятности появления метастазов в костях[32]. С этой целью рекомендуется внутривенное введение Золедроновой кислоты (4 мг в течение не менее 15 минут) каждые 6 месяцев на протяжении 3-5 лет или приём внутрь препарата Клодронат в ежедневной дозе 1600 мг продолжительностью 2-3 года[33]. Адъювантная терапия бифосфонатами больным гормонозависимым раком молочной железы в менопаузе включена в утверждённые в 2017 г. Клинические рекомендации Ассоциации онкологов России[23].
После масштабных испытаний, биологи Базельского университета, выделили вещество, способствующее останавливать распространение метастазов при раке грудной клетке. Это вещество ингибирует Na +/K + ATPase и тем самым диссоциирует кластеры ЦОК (циркулирующие опухолевые клетки).[34]
Виды оперативных вмешательств
Органосохраняющие операции
Органосохраняющие операции — радикальное удаление опухоли в пределах здоровой ткани с удовлетворительным косметическим результатом.
- Лампэктомия.
- Радикальная секторальная резекция (по Блохину).
- Квадрантэктомия с лимфаденэктомией.
- Гемимастэктомия с лимфаденэктомией.
- Субтотальная резекция с лимфаденэктомией.
- Подкожная мастэктомия с лимфаденэктомией.
Радикальные операции
- Радикальная мастэктомия по Мадден.
- Радикальная мастэктомия по Пэйти.
- Радикальная мастэктомия по Холстеду.
- Расширенная радикальная модифицированная мастэктомия.
- Расширенная радикальная подмышечно-грудинная мастэктомия.
- Мастэктомия по Пирогову.
Влияние препаратов, не показанных для лечения РМЖ
Липофильные статины
Липофильный статин Симвастатин снижал риск рецидива рака молочной железы у больных I—III стадий; такая связь не отмечалась при приёме гидрофильных статинов[35].
Бета-адреноблокаторы
Бета-адреноблокаторы могут увеличить длительность безрецидивной выживаемости при трижды негативном раке молочной железы[36].
Влияние пищевых продуктов
Кофе
У пациенток с эстроген-положительным раком молочной железы (ER+), принимавших Тамоксифен и при этом выпивавших 2 и более чашки кофе в день, отмечалась более низкая вероятность рецидива по сравнению с больными, употреблявших меньшее количество кофе[37].
Профилактика
Первичная профилактика рака проводится по следующим направлениям:
- Онкогигиеническая профилактика.
- Биохимическая профилактика.
- Медико-генетическая профилактика.
- Иммунобиологическая профилактика.
- Эндокринно-возрастная профилактика.
Психологические аспекты заболевания
Эмоциональное воздействие на человека, связанное с постановкой диагноза, процедурой лечения и проблемами социальной адаптации, подчас чрезвычайно глубоко.
Большинство цивилизованных клиник, занимающихся профилактикой и лечением раковых заболеваний, работает в сотрудничестве с реабилитационными группами, которые специальными психотерапевтическими методами создают поддерживающие условия с целью подготовки к лечению больных с установленным диагнозом и помощи тем, кто продолжает жизнь после предпринятого лечения.
Существуют и онлайн реабилитационные группы, общение в которых может быть удобно определённой категории больных, в частности тогда, когда они крайне неуверенны в себе, застенчивы и имеют отрицательный образ самих себя, связанный с болезнью. Следует отметить, что часто общение с больными, не профессионалами в медицине, может вызывать неоправданное волнение.
См. также
Примечания
- 1 2 Пак Д. Д., Усов Ф. Н., Фетисова Е. Ю., Волченко А. А., Ефанов В. В. Современные подходы к лечению больных с карциномой in situ молочной железы // Онкология. — 2013. — № 4. — С. 34—39.
- ↑ Маммология. Национальное руководство, 2009, с. 18.
- ↑ Breastfeeding Reduces Risk of Breast Cancer
- 1 2 Кулигина, 2010, с. 203.
- ↑ Маммология. Национальное руководство, 2009, с. 19.
- ↑ Пищевой пластик провоцирует развитие рака груди. MedikForum. Проверено 5 апреля 2016.
- ↑ Кулигина, 2010, с. 203, 205.
- ↑ Wang Y., Klijn J. G., Zhang Y., Sieuwerts A. M., Look M. P., Yang F., Talantov D., Timmermans M., Meijer-van Gelder M. E., Yu J. et al. Gene-expression profiles to predict distant metastasis of lymph-node-negative primary breast cancer // Lancet, 365, 2005. — P. 671—679.
- ↑ Principal manifolds for data cartography and dimension reduction, Leicester, UK, August 2006. A web-page with test microarrays datasets provided for participants of the workshop.
- ↑ Маммология. Национальное руководство, 2009, с. 20.
- ↑ http://www.medines.net/cms/%D1%81%D1%82%D0%B0%D1%82%D1%8C%D0%B8/28-%D1%81%D1%82%D0%B0%D1%82%D1%8C%D0%B8/207-ohzyreniye-riski.html
- ↑ Вирус крупного рогатого скота может повышать риск рака молочной железы у человека. Euroonco.ru. Проверено 14 октября 2015.
- ↑ Leukemia virus in cattle may raise risk for human breast cancer (англ.). Medicalnewstoday. Проверено 14 октября 2015.
- ↑ Белок ELF5 помогает распространяться раку молочной железы. Проверено 19 января 2016.
- ↑ Гистологическая классификация опухолей молочной железы. 2-е изд. — М.: Медицина, 1984. — 31 с.
- ↑ Кулигина, 2010, с. 211—214.
- ↑ American Cancer Society Guidelines for the Early Detection of Cancer.
- ↑ U. S. Preventive Services Task Force: USPTF Breast Cancer Screening recommendations.
- ↑ Kösters J. P., Gøtzsche P. C. Regular self-examination or clinical examination for early detection of breast cancer // Cochrane Database Syst Rev., N 2, 2003. — P. CD003373. — DOI:10.1002/14651858.CD003373. — PMID 12804462.
- ↑ Маммология. Национальное руководство, 2009, с. 227.
- ↑ Черенков В. Г., Тверезовский С. А., Петров А. Б., Фрумкин Б. Б. Инновационные технологии удаления «малых» опухолевых образований молочной железы // Вестник Новгородского гос. ун-та. — 2013. — Т. 71, № 1. — С. 60—63.
- ↑ Лидия Юдина. Заморозить на груди // Аргументы и факты. — 2011. — № 49 за 7 декабря. — С. 62.
- 1 2 Рак молочной железы. Клинические рекомендации Ассоциации онкологов России, 2017.
- ↑ Aromatase inhibitors versus tamoxifen in early breast cancer: patient-level meta-analysis of the randomised trials (англ.) // The Lancet. — 2015-10-03. — Т. 386, вып. 10001. — ISSN 1474-547X 0140-6736, 1474-547X. — DOI:10.1016/S0140-6736(15)61074-1.
- ↑ Jürgen Geisler, Ben Haynes, Gun Anker, Mitch Dowsett, Per Eystein Lønning. Influence of Letrozole and Anastrozole on Total Body Aromatization and Plasma Estrogen Levels in Postmenopausal Breast Cancer Patients Evaluated in a Randomized, Cross-Over Study // Journal of Clinical Oncology. — 2002-02-01. — Т. 20, вып. 3. — С. 751–757. — ISSN 0732-183X. — DOI:10.1200/jco.2002.20.3.751.
- ↑ Elizabeth J. Folkerd, J. Michael Dixon, Lorna Renshaw, Roger P. A'Hern, Mitch Dowsett. Suppression of Plasma Estrogen Levels by Letrozole and Anastrozole Is Related to Body Mass Index in Patients With Breast Cancer // Journal of Clinical Oncology. — 2012-08-20. — Т. 30, вып. 24. — С. 2977–2980. — ISSN 0732-183X. — DOI:10.1200/jco.2012.42.0273.
- ↑ Romond E. H., Perez E. A., Bryant J., et al. Trastuzumab plus adjuvant chemotherapy for operable HER2-positive breast cancer // The New England journal of medicine, 353 (16), 2005. — P. 1673—1684. — DOI:10.1056/NEJMoa052122.
- ↑ Piccart-Gebhart M. J., Procter M., Leyland-Jones B., et al. Trastuzumab after adjuvant chemotherapy in HER2-positive breast cancer // The New England journal of medicine, 353 (16), 2005. — P. 1659—1672. — DOI:10.1056/NEJMoa052306.
- ↑ Семёнова А. И. Основные принципы системной терапии HER2-позитивного рака молочной железы // Практическая онкология. — 2010. — Т. 11, № 4. — С. 239—246.
- ↑ Spread of triple-negative breast cancer could be halted with existing drug.
- ↑ Su Jin Lee, Silvia Park, Hee Kyung Ahn, Jun Ho Yi, Eun Yoon Cho. Implications of Bone-Only Metastases in Breast Cancer: Favorable Preference with Excellent Outcomes of Hormone Receptor Positive Breast Cancer (англ.) // Cancer Research and Treatment. — 2011-06-30. — Т. 43, вып. 2. — С. 89–95. — ISSN 1598-2998. — DOI:10.4143/crt.2011.43.2.89.
- ↑ Early Breast Cancer Trialists' Collaborative Group (EBCTCG). Adjuvant bisphosphonate treatment in early breast cancer: meta-analyses of individual patient data from randomised trials // Lancet (London, England). — 2015-10-03. — Т. 386, вып. 10001. — С. 1353–1361. — ISSN 1474-547X. — DOI:10.1016/S0140-6736(15)60908-4.
- ↑ Sukhbinder Dhesy-Thind, Glenn G. Fletcher, Phillip S. Blanchette, Mark J. Clemons, Melissa S. Dillmon. Use of Adjuvant Bisphosphonates and Other Bone-Modifying Agents in Breast Cancer: A Cancer Care Ontario and American Society of Clinical Oncology Clinical Practice Guideline // Journal of Clinical Oncology. — 2017-03-06. — Т. 35, вып. 18. — С. 2062–2081. — ISSN 0732-183X. — DOI:10.1200/jco.2016.70.7257.
- ↑ Nicola Aceto, Walter Paul Weber, Christoph Rochlitz, Viola Heinzelmann-Schwarz, Christian Kurzeder. Circulating Tumor Cell Clustering Shapes DNA Methylation to Enable Metastasis Seeding (англ.) // Cell. — 2019-01-10. — Т. 176, вып. 1. — С. 98–112.e14. — ISSN 1097-4172 0092-8674, 1097-4172. — DOI:10.1016/j.cell.2018.11.046.
- ↑ Thomas P. Ahern, Lars Pedersen, Maja Tarp, Deirdre P. Cronin-Fenton, Jens Peter Garne. Statin Prescriptions and Breast Cancer Recurrence Risk: A Danish Nationwide Prospective Cohort Study // JNCI: Journal of the National Cancer Institute. — 2011-10-05. — Т. 103, вып. 19. — С. 1461–1468. — ISSN 0027-8874. — DOI:10.1093/jnci/djr291.
- ↑ Amal Melhem-Bertrandt, Mariana Chavez-MacGregor, Xiudong Lei, Erika N. Brown, Richard T. Lee. Beta-Blocker Use Is Associated With Improved Relapse-Free Survival in Patients With Triple-Negative Breast Cancer // Journal of Clinical Oncology. — 2011-07-01. — Т. 29, вып. 19. — С. 2645–2652. — ISSN 0732-183X. — DOI:10.1200/jco.2010.33.4441.
- ↑ Maria Simonsson, Viktoria Söderlind, Maria Henningson, Maria Hjertberg, Carsten Rose. Coffee prevents early events in tamoxifen-treated breast cancer patients and modulates hormone receptor status (англ.) // Cancer Causes & Control. — 2013-05-01. — Vol. 24, iss. 5. — P. 929–940. — ISSN 1573-7225 0957-5243, 1573-7225. — DOI:10.1007/s10552-013-0169-1.
Литература
- Баженова А. П., Островцев Л. Д., Хананашвили Г. Н. Рак молочной железы. — М.: Медицина, 1985. — 272 с.
- Булынский Д. Н., Васильев Ю. С. Современные технологии диагностики и лечения рака молочной железы. — Челябинск: ЧелГМА, 2009. — 84 с. — ISBN 978-5-94507-108-7..
- Кулигина Е. Ш. Эпидемиологические и молекулярные аспекты рака молочной железы // Практическая онкология. — 2010. — Т. 11, № 4. — С. 203—216.
- Летягин В. П., Высоцкая И. В., Легков А. А., Погодина Е. М., Хайленко В. А. Лечение доброкачественных и злокачественных заболеваний молочной железы. — М.: Рондо, 1997. — 287 с.
- Маммология. Национальное руководство / Под ред. В. П. Харченко, Н. И. Рожковой. — М.: ГЭОТАР-Медиа, 2009. — 328 с. — ISBN 978-5-9704-0948-0..
- Черенков В. Г., Тверезовский С. А., Петров А. Б. Опухоли молочной железы. Пути профилактики, ранней диагностики и сохранения груди. — LAMBERT Academic Publishing, 2013. — 164 с. — ISBN 978-3-659-45848-4..
- Chu S. Y., Lee N. C., Wingo P. A., Webster L. A. Alcohol consumption and the risk of breast cancer // American Journal of Epidemiology, 130 (5), 1989. — P. 867—877.
- Friedenreich C. M., Howe G. R., Miller A. B., Jain M. G. A cohort study of alcohol consumption and risk of breast cancer // American Journal of Edidemiology, 137 (5), 1993. — P. 512—520.
- Longnecker M. P., Berlin J. A., Orza M. J., Chalmers T. C. A meta-analysis of alcohol consumption in relation to risk of breast cancer // Journal of the American Medical Association, 260 (5), 1988. — P. 652—656.
- Longnecker M. P. Alcohol consumption in relation to risk of cancers of the breast and large bowel // Alcohol Health & Research World, 16 (3), 1992. — P. 223—229.
- Nasca P. C., Baptiste M. S., Field N. A., Metzger B. B., Black M., Kwon C. S., Jacobson H. An epidemiological case-control study of breast cancer and alcohol consumption // International Journal of Epidemiology, 19 (3), 1990. — P. 532—538.
- Petri A. L. et al. Alcohol intake, type of beverage, and risk of cancer in pre- and postmenopausal women // Alcoholism: Clinical & Experimental Research, 28 (7), 2004. — P. 1084—1090.
- Schatzkin A., Piantadosi S., Miccozzi M., Bartee D. Alcohol consumption and breast cancer: A cross-national correlation study // International Journal of Epidemiology, 18 (1), 1989. — P. 28—31.
- Webster L. A., Layde P. M., Wingo P. A., Ory H. W. Alcohol consumption and risk of breast cancer // Lancet, 2 (8352), 1983. — P. 724—726.
Ссылки
- Новые методы лечения рака молочной железы
- International Agency for Research on Cancer home page
- Australia: Cancer Control Bulletin Alcohol and cancer risk (PDF format)
- Johns Hopkins Avon Foundation Breast Center
- Breast cancer incidence by country
- National Cancer Institute — Breast Cancer Home Page
- Mayo Clinic: How the grading system for cancerous tumors was developed
- Alcohol and the Risk of Breast Cancer Cornell University
- Breast Cancer Treatment Information and Pictures
- State of the Evidence
- RadiologyInfo — The radiology information resource for patients: Breast Cancer
- National Breast Cancer Coalition
- Breast Cancer Action
Для улучшения этой статьи желательно: |
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .