| Глиоксиловая кислота | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Оксоэтановая кислота |
| Традиционные названия | Глиоксиловая кислота, Глиоксалевая кислота |
| Хим. формула | C2H2O3 |
| Физические свойства | |
| Состояние | бесцветная жидкость |
| Молярная масса | 74,04 г/моль г/моль |
| Плотность | 1,34 г/см3 (для 50% водного раствора) |
| Термические свойства | |
| Т. плав. | 80 °C[1] |
| Т. кип. | 111 °C °C |
| Классификация | |
| Рег. номер CAS | 298-12-4 |
| PubChem | 760 |
| Рег. номер EINECS | 206-058-5 |
| SMILES | |
| InChI | |
| ChEBI | 16891 |
| ChemSpider | 740 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Глиоксиловая (или глиоксалевая кислота, оксоэтановая кислота) — органическое вещество, первый член гомологического ряда α-альдегидокислот. Вместе с уксусной, гликолевой, и щавелевой кислотами относится к группе C2 (двууглеродных) карбоновых кислот. Глиоксиловая кислота является бифункциональным соединением и помимо карбоксильной группы содержит карбонильную группу в α-положении, поэтому классифицируется как оксокислота (не следует путать с окси-, или гидроксикислотами).
Строение и физические свойства
В чистом виде выделить глиоксиловую кислоту невозможно, удается получить лишь её моногидрат. Поэтому данной кислоте также приписывают формулу дигидроксиуксусной кислоты CH(OH)2-COOH. Спектроскопия ЯМР показывает, что в водных растворах кислоты устанавливается равновесие между формой диола и полуацеталя [2]:
При нейтральных pH глиоксиловая кислота существует в водном растворе в диссоциированной форме. Сопряженное основание глиоксиловой кислоты называется глиоксилат анион.
Известно значение константы Генри для глиоксиловой кислоты [3]
Получение
Промышленный способ получения глиоксиловой кислоты основан на реакции окисления глиоксаля 65% горячей (40-90°C) азотной кислотой. Основным побочным продуктом в данной реакции является щавелевая кислота, которая отделяется низкотемпературной кристаллизацией. Глиоксаль также может быть окислен до глиоксиловой кислоты на аноде путём электролиза раствора в присутствии хлоридов. Каталитическое окисление этилена или ацетальдегида обладает низкой селективностью, в связи с чем не используется при промышленном получении глиоксиловой кислоты.
Теоретически, возможно получение глиоксиловой кислоты, окислением акрилонитрила перманаганатом калия в кислой среде (KMnO4+H2SO4), но метод не доказан.
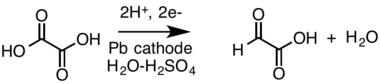
Частичное электровосстановление щавелевой кислоты на катоде, дает достаточно хороший выход реакции (85%), однако связано с техническими трудностями, обусловленными пассивацией свинцового электрода. Данный способ получения глиоксиловой кислоты был предложен в 1904 году швейцарским химиком Юлиусом Тафелем[4][5]:
В качестве эффективного способа получения может быть назван озонолиз малеиновой кислоты[2].
Также глиоксиловую кислоту можно получить гидратацией дихлоруксусной и дибромуксусной кислот [6].
Химические свойства и использование
Как и другие α-альдегидо- и α-кетокислоты глиоксиловая кислота более сильная чем уксусная и пропионовая. Это обусловленно стибилизирующим действием карбонильной группы на анионы α-альдо- и α-кетокислот [7]. Значение константы диссоциации для глиоксиловой кислоты: 4.7 × 10−4 (pKa = 3.33):
- (HO)2CHCOOH (HO)2CHCO2− + H+
При нагревании и реакции с горячими щелочами происходит дисспропорционирование глиоксиловой кислоты с образование гликолевой и щавелевой кислоты или соответствующих солей:
- 2 OCHCOOH + H2O → HOCH2COOH + HOOC–COOH
- 2 OCHCOOH + 3 KOH → HOCH2COOK + KOOC–COOK + 2 H2O
Глиоксиловая кислота легко окисляется азотной кислотой с образованием щавелевой кислоты.
Глиоксиловая кислота проявлет некоторые типичные свойства альдегидов. В частности глиоксалевая кислота образует гетероциклические соединения в реакциях нуклеофильного присоединения с мочевиной, с 1,2-диаминобензолом.
Для глиоксиловой кислоты характерны разнообразные реакции конденсации с фенолами, которые используются в органическом синтезе.
Использование в органическом синтезе
При реакции конденсации с фенолом образуется 4-гидроксиминдальная кислота. Восстановление 4-гидроксоминдальной кислоты позволяет получить 4-гидроксифенилуксусную кислоту, являющуюся важным предшественником в синтезе многих лекарственных препаратов (например при синтезе атенолола).
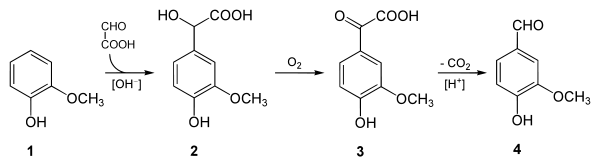
При реакции с гваяколом образуется ванилилминдальная кислота, окислительное декарбоксилирование которой позволяет получить ванилин ("лигниновый способ") [2][8][9].
Глиоксиловая кислота является исходным компонентом при синтезе хелатора иона Fe3+ EHPG (N,N-ethylenebis[2-(2-hydroxyphenyl)glycine])[2]. Комплекс EHPG и трехвалентного железа рассматривается как потенциальное контрастное вещество при магнитнорезонансоном исследовании[10][11].
Также глиоксиловая кислота используется для синтеза 4-гидроксофенилглицина, который является интермедиатом при полусинтетическом получении амоксициллина.
Реакция Хопкинса-Кола на триптофан
Глиоксиловая кислота является одним из компонентов реактива Хопкинса-Кола (Hopkins, Cole). Данный реагент применяется в биохимии для детекции остатков триптофана в белках[12][13][14].
Нахождение и роль в природе
Глиоксиловая кислота содержится в незрелых фруктах, по мере созревания её количество уменьшается [6].
Глиоксиловая кислота является компонентом многих метаболических путей живых организмов. Глиоксилат является интермедиатом глиоксилатного цикла, который позволяет многим живым организмам, таким как бактерии[15], грибы и растения[16] конвертировать жирные кислоты в углеводы. Кроме того в клетках растений глиоксилат образуется в пероксисомах результате окисления гликолата в ходе фотодыхания (гликолатный цикл).
Токсикология
ЛД50 для крыс при оральном введении составляет 2500 мг/кг. Мутагенный эффект не обнаружен[2].
Примечания
- ↑ Merck Index, 11th Edition, 4394
- 1 2 3 4 5 Georges Mattioda and Yani Christidis “Glyoxylic Acid” Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a12_495
- ↑ Ip, H. S. Simon; Huang, X. H. Hilda; Yu, Jian Zhen. “Effective Henry's law constants of glyoxal, glyoxylic acid, and glycolic acid”. Geophysical Research Letters. 36 (1). DOI:10.1029/2008GL036212.
- ↑ Tafel, Julius; and Friedrichs, Gustav (1904). “Elektrolytische Reduction von Carbonsäuren und Carbonsäureestern in schwefelsaurer Lösung”. Berichte der deutschen chemischen Gesellschaft. 37 (3): 3187–3191. DOI:10.1002/cber.190403703116. Проверено 19 December 2013.
- ↑ Cohen, Julius. Practical Organic Chemistry 2nd Ed.. — London : Macmillan and Co. Limited, 1920. — P. 102-104.
- 1 2 Грандберг И.И. Органическая химия: Учб. для студ. вузов - М.: Дрофа, 2004. - 672 с. ISBN 5-7107-8771-X
- ↑ Травень В.Ф. Органическая химия: учебник для вузов: в 2 т. - М.: ИКЦ "Академкнига", 2008. - ISBN 978-5-94628-318-2
- ↑ Fatiadi, Alexander; and Schaffer, Robert (1974). “An Improved Procedure for Synthesis of DL-4-Hydroxy-3-methoxymandelic Acid (DL-"Vanillyl"-mandelic Acid, VMA)” (PDF). Journal of Research of the National Bureau of Standards - A. Physics and Chemistry. 78A (3): 411–412. DOI:10.6028/jres.078A.024. Проверено 19 December 2013. Символ переноса строки в
|title=на позиции №39 (справка) - ↑ Kamlet, Jonas; and Mathieson, Olin. Manufacture of vanillin and its homologues U.S. Patent 2,640,083. — U.S. Patent Office, 1953.
- ↑ Kuźnik N, Jewuła P, Oczek L, Kozłowicz S, Grucela A, Domagała W. (2014). “EHPG iron(III) complexes as potential contrast contrast agents for MRI”. Acta Chim Slov. 61: 87–93. PMID 24664331.
- ↑ Liu GC, Wang YM, Jaw TS, Chen HM, Sheu RS. (1993). “Fe(III)-EHPG and Fe(III)-5-Br-EHPG as contrast agents in MRI: an animal study”. J Formos Med Assoc. 92: 359–366. PMID 8104585.
- ↑ R.A. Joshi. Question Bank of Biochemistry. — New Age International, 2006. — P. 64. — ISBN 978-81-224-1736-4.
- ↑ Debajyoti Das. Biochemistry. — Academic Publishers, 1980. — P. 56. — ISBN 978-93-80599-17-5.
- ↑ P. M. Swamy. Laboratory Manual on Biotechnology. — Rastogi Publications, 2008. — P. 90. — ISBN 978-81-7133-918-1.
- ↑ Holms WH (1987). “Control of flux through the citric acid cycle and the glyoxylate bypass in Escherichia coli”. Biochem Soc Symp. 54: 17—31. PMID 3332993.
- ↑ Escher CL, Widmer F (1997). “Lipid mobilization and gluconeogenesis in plants: do glyoxylate cycle enzyme activities constitute a real cycle? A hypothesis”. Biol Chem. 378 (8): 803—813. PMID 9377475.
Ссылки
- Колотов С.С., Менделеев Д. И. Глиоксалевая кислота // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .
![{\displaystyle {\ce {2CH(HO)2-COOH <=> O[(HO)CH-COOH]2{+}H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af7ad02a4d960433307a4aef58367440ca43a5ee)
![{\displaystyle K_{H}=1.09\times 10^{4}\times \exp[(40.0\times 10^{3}/R)\times (1/T-1/298)]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3b877b00a51f022e292a5054ebe2bf9dc553c440)