Эта статья или раздел нуждается в переработке. |
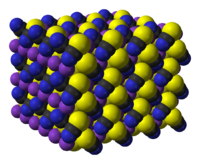
| Тиоцианат калия | |
|---|---|
| | |
 | |
| Общие | |
| Традиционные названия | роданид калия |
| Хим. формула | KSCN |
| Физические свойства | |
| Состояние | бесцветные кристаллы без запаха острого горьковатого вкуса (ядовит) |
| Молярная масса | 97,18 г/моль |
| Плотность | 1,886 г/см³ |
| Термические свойства | |
| Т. плав. | 173,2 °C |
| Т. разл. | ниже 500 °C |
| Энтальпия образования | −203,4 кДж/моль |
| Химические свойства | |
| Растворимость в воде |
(при 0 °C) 177 (20 °C) 217 г/100 мл |
| Растворимость в ацетоне | 21,0 г/100 мл |
| Классификация | |
| Рег. номер CAS | 333-20-0 |
| PubChem | 516872 |
| Рег. номер EINECS | 206-370-1 |
| SMILES | |
| InChI | |
| RTECS | XL1925000 |
| ChEBI | 30951 |
| ChemSpider | 9150 |
| Безопасность | |
| ЛД50 | 854 мг/кг |
| Токсичность |
 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Тиоциана́т ка́лия (родани́д ка́лия) — химическое соединение, калиевая соль тиоциановой кислоты. Химическая формула — KSCN.
Свойства
На вид — бесцветные кристаллы. Не имеют запаха. Гигроскопичны.
Тиоцианат калия реагирует с бромной водой с образованием бромциана и сульфата калия, с железом с образованием цианида калия и сульфида железа. Разлагается при нагревании выше 250 °C — до сульфида калия и циана, выше 300 °C — дисульфида калия и цианида калия.
Энтальпия плавления ΔH°пл. (кДж/моль): 10,5
Растворимость
| Вещество | (в г/100 г или характеристика) |
|---|---|
| амиловый спирт | растворим |
| вода (0 °C) | 177 |
| вода (20 °C) | 217 |
| вода (25 °C) | 239 |
| вода (32,5 °C) | 265 |
| вода (47,3 °C) | 317 |
| вода (67 °C) | 408 |
| вода (99 °C) | 673 |
| этанол | растворим |
Получение
Роданистый калий можно получить при взаимодействии роданистого аммония с гидроксидом калия:
NH4SCN + KOH = KSCN + NH3 + H2O
В горячий (70 °С) раствор 500 г NH4NCS (ч. д. а.) в 250 мл воды приливают (под тягой) при перемешивании раствор 368 г KOH (ч.) в 400 мл воды. Смесь нагревают при 80—85 °С до полного удаления NH3 (проба раствора при нагревании с KOH не должна выделять NH3, обнаруживаемого по запаху). По окончании реакции раствор фильтруют через двойной складчатый фильтр. Фильтрат упаривают до образования пленки кристаллов и охлаждают. Выпавшие кристаллы отсасывают на воронке Бюхнера и сушат при 30-40 °С. Выход 400—440 г (62—70 %) препарата, соответствующего реактиву квалификации ч. д. а. Из маточного раствора упариванием и кристаллизацией можно получить еще 100—140 г соли.
Если в качестве сырья применяют технический продукт NH4NCS, содержащий значительную примесь сульфатов, то методика приготовления KNCS несколько иная.
К нагретому до 80 °С раствору 175 г NH4NCS в 50 мл воды добавляют Ba(OH)2 до полного осаждения SO42-. Раствору дают отстояться и фильтруют. Фильтрат нагревают до 80 °С и прибавляют малыми порциями K2CO3 (ч.) до слабощелочной реакции на фенолфталеин. Затем реакционный раствор кипятят 10—12 ч до удаления NH3, вносят 2 г активного угля и упаривают до тех пор, пока плотность раствора не станет равной 1,45 (при 110 °С). Раствор фильтруют и охлаждают. Выпавшие кристаллы отсасывают на воронке Бюхнера и сушат при 30—40 °С.
Выход 100 г (47 %). Используя маточный раствор, можно значительно повысить выход препарата.
Применение
- Образует с Fe3+ кроваво-красное комплексное соединение, благодаря чему используется как аналитический реагент на соли трёхвалентного железа, а также как имитатор крови в фокусах и кино:
- [Fe(H2O)6]3+ + SCN− ⇌ [Fe(SCN)(H2O)5]2+ + H2O.
Токсичность
Тиоцианат калия ядовит. Смертельная доза — 854 мг/кг.
Ссылки
См. также
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .
