| Нитрид трииода | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Иодид азота |
| Хим. формула | NI3 |
| Физические свойства | |
| Состояние | кристаллы |
| Молярная масса | 394.77 г/моль |
| Термические свойства | |
| Т. кип. | возгоняется при - 20 °C |
| Т. разл. | от 0 до 25 С |
| Классификация | |
| Рег. номер CAS | 13444-85-4 |
| PubChem | 61603 |
| SMILES | |
| InChI | |
| ChemSpider | 55511 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
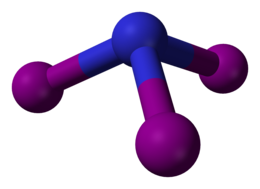
Нитри́д триио́да (иногда йодистый азот, ошиб. азид йода) — чрезвычайно взрывчатое неорганическое соединение с формулой NI3. Обычно известен в виде чёрно-коричневых кристаллов — аддукта с аммиаком NI3·nNH3 (аммиаката), но был получен и в индивидуальном виде реакцией BN с IF при низких температурах.
Представляет собой чёрные кристаллы, очень чувствительные к механическим воздействиям. В сухом виде взрывается от прикосновения, образуя розовато-фиолетовое облако паров йода. Это единственное вещество, которое взрывается под воздействием альфа-частиц и других продуктов ядерного распада[1].
Свойства
Аддукт нитрида иода разлагается при взаимодействии с диэтилцинком:
- NH3·NI3 + 3Zn(C2H5)2 → NH3 + N(C2H5)3 + 3ZnC2H5I
Благодаря именно этой реакции установлено строение аддукта йодида азота с аммиаком http://pubs.rsc.org/en/content/articlepdf/1905/ct/ct9058700055[2]
Во влажном виде при наличии избытка аммиака в растворе сравнительно устойчив. Единственное известное взрывчатое вещество, способное сдетонировать от альфа-излучения. Из-за крайней нестабильности применяется исключительно как эффектный химический фокус.
Нестабильность вещества вызвана большой длиной связи N—I и огромными размерами трёх атомов иода, приходящихся на один атом азота, и соответственно низкой энергией активации реакции разложения.
Нерастворим в этаноле. Разлагается горячей водой, кислотами-окислителями, щелочами.
Разложение чистого вещества протекает по следующей реакции:
- 2NI3(тв.) → N2↑ + 3I2↑ ΔH = −290 кДж/моль
Аммиак, который присутствует в аддукте, является восстановителем для образующегося иода:
- 8NI3·NH3 → 5N2 + 6NH4I + 9I2
Нитрид трииода подвергается гидролизу с образованием оксида азота (III) и йодоводородной кислоты:
- 2NI3 + 3H2O → 6HI + N2O3
Получение
Получают взаимодействием водного раствора аммиака (нашатырный спирт) — обычно 25% и спиртового раствора иода в соотношении 1:2. При смешивании выпадает чёрный или бурый осадок, представляющий собой продукт присоединения аммиака к нитриду трииода.
- 3I2 + 5NH4OH → 3NH4I + NH3•NI3↓ + 5H2O
Возможно использование кристаллического иода вместо раствора, в этом случае кристаллы иода поливают раствором аммиака. При реакции с безводным аммиаком в условиях низких температур образующийся продукт имеет состав NI3·(NH3)5, при нагревании он начинает терять часть аммиака.
Осадок может быть очищен от примеси аммиака промыванием спиртом, но при этом его детонационная чувствительность сильно возрастает.
Литература
- Silberrad, O. (1905). “The Constitution of Nitrogen Triiodide”. Journal of the Chemical Society, Transactions. 87: 55—66. DOI:10.1039/CT9058700055.
Примечания
- ↑ Bowden, F. P. (1958). “Initiation of Explosion by Neutrons, α-Particles, and Fission Products”. Proceedings of the Royal Society of London A. 246 (1245): 216—219. DOI:10.1098/rspa.1958.0123.
- ↑ Oswald Silberrad. IX.—The constitution of nitrogen iodide (англ.) // J. Chem. Soc., Trans.. — 1905-01-01. — Vol. 87, iss. 0. — P. 55–66. — ISSN 0368-1645. — DOI:10.1039/ct9058700055.
| Это заготовка статьи о неорганическом веществе. Вы можете помочь проекту, дополнив её. |
Для улучшения этой статьи желательно: |
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .