| Оксид мышьяка | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Arsenic trioxide |
| Хим. формула | As2O3 |
| Физические свойства | |
| Молярная масса | 197.841 г/моль |
| Плотность | 3.74 г/см³ |
| Классификация | |
| Рег. номер CAS | 1327-53-3 |
| PubChem | 261004 |
| Рег. номер EINECS | 215-481-4 |
| SMILES | |
| InChI | |
| RTECS | CG3325000 |
| ChEBI | 30621 |
| ChemSpider | 229103 |
| Безопасность | |
| ЛД50 | 14,6 мг/кг (крысы, орально) |
| Токсичность | чрезвычайно токсичен |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Оксид мышьяка(III) — неорганическое соединение с химической формулой As2O3, являющееся ценным химическим сырьём для получения других производных мышьяка, в том числе мышьяксодержащих органических соединений. Валовой объём производства в мире — 50 000 тонн в год[1]. Однако безопасность применения во многих областях подвергается сомнению из-за высокой токсичности данного вещества.
Получение и свойства
Оксид мышьяка(III) может быть получен многими способами, включая окисление (горение) мышьяка и его производных на воздухе. Показательна реакция разложения аурипигмента, сульфида мышьяка:
Большая часть, однако, является побочным продуктом других производств — золотодобычи и получения меди, где он выделяется при прокаливании на воздухе, что приводило к многочисленным массовым отравлениям[2]. В настоящее время интенсивная добыча мышьяковых руд ведётся только в Китае[1].
Оксид мышьяка(III) является амфотерным оксидом, его раствор обладает слабокислой реакцией. В щелочных растворах образует арсениты, в концентрированной соляной кислоте даёт хлорид мышьяка(III). Только сильнейшие окислители — озон, пероксид водорода, азотная кислота — способны превратить его в оксид мышьяка(V) As2O5 или — при понижении концентрации — арсин (AsH3) в зависимости от условий реакции.
Структура
В жидком и газообразном (до 800 °C) состояниях имеет формулу As4O6 (в форме димера) и изоструктурен P4O6). При нагреве свыше 800 °C As4O6 распадается на молекулы As2O3, схожий по строению с N2O3. В твёрдом состоянии сосуществуют три полиморфных формы: кубический молекулярный As4O6 и две полимерные формы. Полимеры, образующие при остывании монокристаллы, напоминают пирамидальную структуру AsO3 с общими атомами кислорода.[3]
 |  | 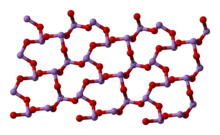 |
(cubic) | (monoclinic) | (monoclinic) |
Использование
Оксид мышьяка(III) используется для изготовления цветного стекла, также применяется в лесохимии и электротехнике полупроводников[1], получения чистого мышьяка и его соединений, таких как какодилат натрия и арсенид натрия.
В соединении с ацетатом меди(II)[1] триоксид образует красящее вещество — парижскую зелень, ныне из-за чрезвычайной токсичности неиспользуемую.
Применение в медицине
Используется с древнейших времён в китайской медицине[4], а также (с XIX века) в гомеопатии. В конвенциональной медицине триоксид мышьяка используется для лечения злокачественных опухолей, таких как лейкемия, однако ввиду высоких рисков его применения предпочтение отдаётся другим препаратам[5][6][7].
Также триоксид успешно лечит аутоиммунные заболевания[8], взаимодействует с ферментом тиоредоксиновая редуктаза[9].
Обнаружение в природе
As2O3 содержится в арсенолите и клаудетите.
Токсикология

Оксид мышьяка (III) очень ядовит. Токсичность триоксида стала легендарной и широко описана в литературе[10][11][11][12].
В Австрии жили «мышьякоеды», получавшие дозы во много раз больше смертельной без особого вреда для здоровья. Считается, что мышьяк повышает работоспособность, особенно при работе на больших высотах[13][14][15].
ПДК для неорганических соединений мышьяка, включая As2O3, составляет 0.010 мг/м³.
Полулетальная доза — 19,1 мг/кг.[источник не указан 951 день]
Примечания
- 1 2 3 4 Sabina C. Grund, Kunibert Hanusch, Hans Uwe Wolf «Arsenic and Arsenic Compounds» in Ullmann’s Encyclopedia of Industrial Chemistry, VCH-Wiley, 2008, Weinheim. (англ.)
- ↑ Giant Mine - Northwest Territories Region - Indian and Northern Affairs Canada (недоступная ссылка). Проверено 28 августа 2007. Архивировано 2 апреля 2012 года. (англ.)
- ↑ Holleman, A. F.; Wiberg, E. «Inorganic Chemistry» Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- ↑ Marcel Gielen, Edward R. T. Tiekink. Metallotherapeutic Drugs and Metal-Based Diagnostic Agents. — Wiley, 2005. — P. 298.
- ↑ Steven L. Soignet; et al. (2001). “United States Multicenter Study of Arsenic Trioxide in Relapsed Acute Promyelocytic Leukemia”. Journal of Clinical Oncology. 19 (18): 3852—3860.
- ↑ Antman, K. H. (2001). “Introduction: The history of arsenic trioxide in cancer therapy”. Oncologist. 6(Suppl. 2) (1—2): 2006.
- ↑ Jun Zhu, Zhu Chen,Valérie Lallemand-Breitenbach, Hugues de Thé "How Acute Promyelocytic Leukaemia Revived Arsenic, " Nature Reviews Cancer 2002, volume 2, 1-9.
- ↑ Bobé Pierre, Bonardelle Danielle, Benihoud Karim, Opolon Paule, Chelbi-Alix Mounira (2006). “Arsenic trioxide: A promising novel therapeutic agent for lymphoproliferative and autoimmune syndromes in MRL/lpr mice”. Blood. 108 (13): 3967-3975.
- ↑ Lu J, Chew EH, Holmgren A (2007). “Targeting thioredoxin reductase is a basis for cancer therapy by arsenic trioxide”. Proc. Natl. Acad. Sci. U.S.A. 104 (30): 12288—93. DOI:10.1073/pnas.0701549104. PMID 17640917.
- ↑ Stanton v Benzler 9716830. U.S. 9th Circuit Court of Appeals (17 июня 1998). — «(...) convicted by a jury of first degree murder for poisoning her ex-husband. Her ex-husband's body was found with traces of arsenic trioxide in it.». Проверено 9 июня 2008. Архивировано 2 апреля 2012 года.
- 1 2 Emsley, John. Arsenic // The Elements of Murder: A History of Poison. — Oxford University Press, 2006. — P. 93 –197. — ISBN 9780192806000.
- ↑ Madame Bovary by Flaubert
- ↑ Arsenic Eaters — New York Times July 26, 1885
- ↑ Richard M. Allesch. Arsenik. Seine Geschichte in Österreich. 54. Band. Klagenfurt: Kleinmayr 1959.
- ↑ G. Przygoda, J. Feldmann, W. R. Cullen (2001). “The arsenic eaters of Styria: a different picture of people who were chronically exposed to arsenic”. Applied Organometallic Chemistry. 15 (6): 457—462. DOI:10.1002/aoc.126.
Ссылки
- На английском языке
- Solubility of As2O3 in water as function of temperature
- Case Studies in Environmental Medicine: Arsenic Toxicity
- IARC Monograph — Arsenic and Arsenic Compounds
- International Chemical Safety Card 0378
- NIOSH Pocket Guide to Chemical Hazards
- NTP Report on Carcinogens — Inorganic Arsenic Compounds
- Use of Arsenic Trioxide in Multiple Myeloma Treatment
- The use of Arsenic trioxide in medicine.
- Institute of Chemistry Austria, speciallised on arsenic and various arsenic compounds
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .
