| Пентаэритрит | |
|---|---|
 | |
 | |
 | |
| Общие | |
| Систематическое наименование |
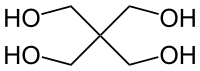
2,2-бис(гидроксиметил)пропан-1,3-диол |
| Традиционные названия | пентаэритрит |
| Хим. формула | C5H12O4 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 136,15 г/моль |
| Плотность | 1,394 г/см³ |
| Термические свойства | |
| Т. плав. | 260,5 °C |
| Т. субл. | 500 ± 1 градус Фаренгейта[1] |
| Т. кип. | 276 (30 мм.рт.ст.) °C |
| Т. всп. | 470 °C |
| Энтальпия образования | -948 кДж/моль |
| Давление пара | 8,0E-8 ± 1,0E-8 мм рт.ст.[1] |
| Химические свойства | |
| Растворимость в воде | 5,6 г/100 мл |
| Классификация | |
| Рег. номер CAS | 115-77-5 |
| PubChem | 8285 |
| Рег. номер EINECS | 204-104-9 |
| SMILES | |
| InChI | |
| RTECS | RZ2490000 |
| ChemSpider | 7984 |
| Безопасность | |
| Токсичность | не образует токсичных соединений с другими веществами в воздушной среде и сточных водах |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Пентаэритри́т (2,2-бис(гидроксиметил)пропан-1,3-диол) C(CH2OH)4 — четырёхатомный спирт с углеродным скелетом неопентана.
Физические свойства
Белый кристаллический порошок со сладким вкусом. Растворимость вещества в воде (% по массе) составляет: 5,56 (15 °C), 7,1 (25 °C), 19,3 (55 °C), 76,6 (100 °C). Растворимость в других растворителях (% по массе) при 100 °С: в этиленгликоле — 12,9, в глицерине — 10,3, в формамиде — 21, в пиридине — 3,7.[2] Температура кипения 276 °C при 30 мм.рт.ст., возгоняется.
Химические свойства
Пентаэритрит проявляет свойства спиртов: алкилируется, ацилируется, реагирует с азотной кислотой с образованием моно-, ди-, три- и тетрапроизводных; образует алкоголяты и комплексы с металлами. Отличительной чертой пентаэритрита является способность образовывать циклические производные. Так при реакции с тионилхлоридом, в зависимости от условий, образует моно-, ди-, трихлорпроизводное или пентаэритритдисульфит:
Также пентаэритрит может реагировать с альдегидами и кетонами в кислой среде с образованием моно- и бициклического продукта:
Получение
Пентаэритрит получают конденсацией формальдегида с ацетальдегидом при катализе щелочами и избытке формальдегида, при этом на первой стадии происходит альдольная конденсации с образованием трис-метилолацетальдегида, который далее в перекрестной реакции Канниццаро восстанавливается формальдегидом до пентаэритрита[3]:
Применение
Пентаэритрит применяется в производстве алкидных смол, пентафталевых лаков и эмалей, синтетических смазочных масел, пентапласта, пластификаторов и антиоксидантов для полимеров, термостабилизаторов, для синтеза ПАВ, взрывчатого вещества тетранитропентаэритрита (ТЭНа).
Примечания
- 1 2 http://www.cdc.gov/niosh/npg/npgd0485.html
- ↑ Химическая энциклопедия, т.3, под ред. Кнунянца И. Л., Москва, Большая Российская Энцилопедия, стр. 462
- ↑ Органикум. Том 2. Москва, Мир, 1992, стр. 202—203
Ссылки
- ГОСТ 9286-2012. Пентаэритрит технический. Технические условия
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .


