Атомная теория — физическая теория, предполагающая, что всё на свете состоит из мельчайших частиц — атомов, скреплённых между собой ядерными и электрическими силами. В XX веке на практике было доказано, что атом можно разделить на ещё более мелкие — субатомные — частицы.
История
Атомизм
В древнегреческой философии, а позднее и в средние века, люди предполагали, что вещи вокруг них состоят из двух частей: неделимые атомы, каким-то образом сцепленные друг с другом, и из пустоты между атомами. Атомы считались вечными и неразрушимыми корпускулами.[1][2] Эта позиция была отражена в трудах таких философов, как Демокрит или Левкипп, но никаких доказательств этой теории в то время не было.
Первая теория строения атома
В конце XVIII века были открыты химические законы сохранения:
- Закон сохранения массы, открытый в 1789 году Антуаном Лораном Лавуазье, гласит, что масса реактивов во время химической реакции не меняется;[3]
- Закон постоянства состава, открытый в 1799 году Жозефом Луи Прустом, гласит, что любое определённое химическое соединение, не зависимо от способа его получения, состоит из одних и тех же химических элементов;[4]
- Закон кратных отношений, открытый в 1803 году Джоном Дальтоном, гласит, что отношения масс одного элемента к другому будет целым числом.[5]

Для выполнения этих законов материя должна обладать дискретной структурой. Но в то время была не совсем ясна структура того, что сейчас мы называем «молекулой». В 1811 году Амедео Авогадро провёл серию опытов с газом и выяснил, что два литра водорода реагируют только с одним литром кислорода при получении водяного пара.[6] В результате исследования броуновского движения открытого в 1827 году [7] стало очевидно, что материя состоит из отдельных частиц — атомов, способных собираться в группы — молекулы, то есть была создана атомная теория строения вещества.
Открытие субатомных частиц
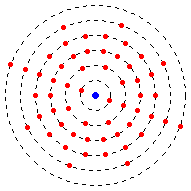
До 1897 года атомы считались неделимыми. В 1897 году Джозеф Джон Томсон провёл опыт с круксовой трубкой,[8] в котором впервые наблюдался электрон. На катод подавалось некое напряжение и, как впоследствии оказалось, в таких условиях катод излучает пучки электронов. Томсон выяснил, что эти пучки отклоняются при воздействии на них электромагнитным полем. Сам Томсон называл эти частицы корпускулами, но позднее им дали отдельное имя — электроны.
Открытие ядра атома
Модель атома Томсона была опровергнута в 1909 году учеником Томсона — Эрнестом Резерфордом. Последний обнаружил, что атом не однороден по своей структуре: в центре находится массивное положительное плотное ядро, а вокруг него, как планеты вокруг Солнца, летают электроны.
Оказалось, если обстреливать альфа-частицами тонкий лист золота, то альфа-частицы будут отклоняться на разные углы, причём часть из них — на угол больше а такое может быть только если массивная положительная альфа-частица встречает на своём пути достаточно массивное положительное препятствие.[9]
Создание квантовой теории атома
У планетарной модели был ряд недостатков, из которых самым существенным был недостаток, связанный с теоретически верной потерей энергии электрона: так как электрон вращается вокруг атома, то на него действует центростремительное ускорение, а по формуле Лармора любая заряженная частица, движущаяся с ускорением, излучает. То есть теряет энергию. А если электрон теряет энергию, то в конце концов он должен упасть на ядро, чего в реальности не происходит.
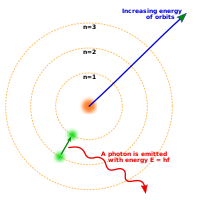
В 1913 году Нильс Бор предположил, что электрон может вращаться не как угодно, а на строго определённых орбитах, не меняя своей энергии сколь угодно долгое время. Переход с орбиты на орбиту требует определённой энергии — кванта энергии.
Открытие изотопов
В 1907 году радиохимиком Фредериком Содди было обнаружено, что существуют вещества с одинаковыми химическими свойствами, но отличающиеся числом нейтронов.
Открытие делимости ядра
В 1930 году было обнаружено, что если высокоэнергетичные альфа-частицы попадают на некоторые лёгкие элементы, то последние излучают лучи с необычно большой проникающей способностью. Это излучение обладает гораздо большей проникающей способностью, чем все известные остальные лучи. В 1932 году Ирен и Фредерик Жолио-Кюри показали, что если это неизвестное излучение попадает на парафин, то образуются протоны высоких энергий, не сходящиеся с теоретическими расчётами. Физик Джеймс Чедвик предположил, что это излучение состоит из незаряженных частиц с массой, близкой к массе протона, и провёл серию экспериментов[каких?], подтвердивших эту гипотезу. Эти незаряженные частицы были названы нейтронами.
Открытие атомных орбиталей

В 1924 году Луи Де Бройлем было предположено, что все частицы связаны с волной, названной впоследствии волной де Бройля с частотой и с длиной волны
В 1926 году было записано уравнение Шрёдингера,[10] описывающее субатомные частицы как волны. Чуть позже Макс Борн предположил, что корпускулярно-волновой дуализм верен не только для фотонов, но и в принципе для всех частиц. Было введено понятие орбитали — место наиболее вероятного нахождения электрона данного атома. Ведь теоретически электрон может быть очень редко обнаружен на любом расстоянии от атома,[11] но чаще всего он находится где-то рядом с оным, как раз «на орбитали».
Теория строения атома в культуре
- Достаточно известно высказывание Р. Фейнмана:
| Если бы в результате какой-то мировой катастрофы все накопленные научные знания оказались бы уничтоженными, и к грядущим поколениям живых существ перешла бы только одна фраза, то, какое утверждение, составленное из наименьшего числа слов, принесло бы наибольшую информацию?
Я считаю, что это – атомная гипотеза: все тела состоят из атомов - маленьких телец, которые находятся в беспрерывном движении, притягиваются на небольших расстояниях, но отталкиваются, если одно из них плотнее прижать к другому. В одной этой фразе содержится невероятное количество информации о мире, стоит лишь приложить к ней немного воображения и чуть соображения.Р. Фейнман. |
- Модель атома в упрощёном виде является одним из известных символов науки.
Примечания
- ↑ Aristotle, Metaphysics I, 4, 985b 10—15.
- ↑ Berryman, Sylvia, «Ancient Atomism», The Stanford Encyclopedia of Philosophy (Fall 2008 Edition), Edward N. Zalta (ed.), http://plato.stanford.edu/archives/fall2008/entries/atomism-ancient/
- ↑ Weisstein, Eric W. Lavoisier, Antoine (1743-1794)]. scienceworld.wolfram.com. Проверено 1 августа 2009. Архивировано 7 апреля 2013 года.
- ↑ Proust, Joseph Louis. «Researches on Copper», excerpted from Ann. chim. 32, 26-54 (1799) [as translated and reproduced in Henry M. Leicester and Herbert S. Klickstein, A Source Book in Chemistry, 1400—1900 (Cambridge, MA: Harvard, 1952)]. Retrieved on August 29, 2007.
- ↑ Andrew G. van Melsen. From Atomos to Atom. — Mineola, N.Y. : Dover Publications, 1952. — ISBN 0-486-49584-1.
- ↑ Avogadro, Amedeo (1811.). “Essay on a Manner of Determining the Relative Masses of the Elementary Molecules of Bodies, and the Proportions in Which They Enter into These Compounds”. Journal de Physique. 73: 58—76. Проверьте дату в
|year=(справка на английском) - ↑ Einstein, A. (1905). “Über die von der molekularkinetischen Theorie der Wärme geforderte Bewegung von in ruhenden Flüssigkeiten suspendierten Teilchen”. Annalen der Physik. 322 (8): 549. Bibcode:1905AnP...322..549E. DOI:10.1002/andp.19053220806.
- ↑ Thomson, J.J. (1897). “Cathode rays” ([facsimile from Stephen Wright, Classical Scientific Papers, Physics (Mills and Boon, 1964)]). Philosophical Magazine. 44 (269): 293. DOI:10.1080/14786449708621070.
- ↑ Geiger, H (1910). “The Scattering of the α-Particles by Matter”. Proceedings of the Royal Society. A 83: 492—504.
- ↑ Schrödinger, Erwin (1926). “Quantisation as an Eigenvalue Problem”. Annalen der Physik. 81 (18): 109—139. Bibcode:1926AnP...386..109S. DOI:10.1002/andp.19263861802.
- ↑ Mahanti, Subodh. Max Born: Founder of Lattice Dynamics. Архивировано 22 января 2009 года. Проверено 1 августа 2009.
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .


