| Фактор роста фибробластов | |
|---|---|
 Результат анализа кристаллической структуры комплекса fgf10-fgfr2b | |
| Идентификаторы | |
| Символ | FGF |
| Pfam | PF00167 |
| Pfam clan | CL0066 |
| InterPro | IPR002348 |
| PROSITE | PDOC00220 |
| SCOP | 1bas |
| SUPERFAMILY | 1bas |
| Доступные структуры белков | |
| Pfam | структуры |
| PDB | RCSB PDB; PDBe; PDBj |
| PDBsum | 3D-модель |
Факторы роста фибробластов, или FGFs, относятся к семейству факторов роста, участвующих в ангиогенезе, заживлении ран и эмбриональном развитии. Факторы роста фибробластов — это гепарин-связывающие белки. Было доказано, что взаимодействия с расположенными на поверхности клеток протеогликанами необходимы для передачи сигнала факторов роста фибробластов. Факторы роста фибробластов играют ключевую роль в процессах пролиферации и дифференцировки широкого спектра клеток и тканей.
Семейства
У человека было обнаружено 22 члена семейства FGF, все они — структурно сходные сигнальные молекулы:[1][2][3]
- Представители факторов роста с FGF1 до FGF10 все связывают рецепторы фактора роста фибробластов (FGFRs). FGF1 также известен как кислый, а FGF2 — как основной фактор роста фибробластов.
- Было доказано, что представители FGF11, FGF12, FGF13 и FGF14, также известные как гомологические факторы 1 — 4 (FHF1-FHF4), имеют четко выраженные функциональные отличия от FGFs. Хотя эти факторы обладают удивительно схожими гомологиями последовательности, они не связывают рецепторы фактора роста (FGFRs) и участвуют во внутриклеточных процессах, связанных с FGFs.[4]
Эта группа также известна как «iFGF»[5]
- Представители с FGF16 по FGF23 — новые и не так хорошо изучены. FGF15 — крысиный ортолог человеческого белка FGF19 (следовательно, у человека нет FGF15[источник не указан 940 дней]).
- Человеческий FGF20 был обнаружен на основании его гомологии с FGF-20 (XFGF-20) ксенопуса.[6][7]
- В отличие от локального действия других FGF, FGF15/FGF19, FGF21 и FGF23 имеют больше системных эффектов[8] и объединяются в группу эндокринных FGF[9].
Рецепторы
Семейство рецепторов фактора роста фибробластов у млекопитающих имеет четыре представителя: FGFR1, FGFR2, FGFR3, и FGFR4. FGFRs состоят из трех типов внеклеточных иммуноглобулиновых доменов (D1-D3), односпирального трансмембранного домена и внутриклеточного тирозинкиназного домена. FGFs взаимодействует с D2 и D3 доменами; взаимодействия с D3 в первую очередь ответственны за специфичное связывание лигандов. Связь гепарансульфата осуществляется посредством домена D3. Короткий отрезок кислых аминокислот, расположенный между доменами D1 и D2, имеет автоингибирующие функции. Этот мотив «кислотного бокса» («acid box») взаимодействует с гепарансульфатом в месте связывания для предотвращения активации рецептора при отсутствии факторов роста фибробластов.
Альтернативный сплайсинг мРНК приводит к появлению 'b' и 'с' вариантов рецепторов фактора роста FGFRs 1, 2 и 3. С помощью этого механизма семь различных подтипов рецепторов фактора роста могут быть экспрессированы на поверхности клетки. Каждый рецептор фактора роста, FGFR, обычно связывает несколько разных FGFs. Точно так же наибольшее число FGFs может связываться с несколькими различными подтипами FGFR. FGF1 иногда рассматривают как «универсальный лиганд», поскольку он способен активировать все семь различных подтипов FGFRs. В отличие от него, FGF7 (фактор роста кератиноцитов, KGF) связывается только с FGFR2b (KGFR).
Сигнальный комплекс на поверхности клетки, как полагают, является тройным комплексом, сформировавшимся между двумя одинаковыми лигандами FGF, двумя субъединицами FGFR и одной либо двумя цепями гепарансульфата.
Блокирование рецептора фактора роста фибробластов 1 типа (моноклональное антитело OM-RCA-01) или рецептора фактора роста фибробластов 2 типа (RPT835) приводит к подавлению пролиферации клеток рака.
История
Фактор роста фибробластов был найден Армелиным (Armelin) в вытяжке из гипофиза в 1973 году[10], затем также был обнаружен Господаровичем (Gospodarowicz) и др. в мозге коровы. Были проведены биопробы, в ходе которых фибробласты стали быстро расти (первый доклад был опубликован в 1974).[11]
В дальнейшем вытяжка была фракционирована с использованием кислотного и щелочного рН, и были выделены две немного отличающиеся формы, которые получили название «кислотный фактор роста фибробластов» (FGF1) и «основной фактор роста фибробластов» (FGF2). Эти белки имели высокую степень сходства аминокислотного состава, но были различными митогенами. У человека FGF2 встречается в виде четырёх изоформ — одной с низкой молекулярной массой (LMW) и трех с высокой молекулярной массой (HMW).[12] LMF прежде всего цитоплазматическая и функционирует аутокринным способом, в то время как HMF FGF2 ядерная и проявляет активность посредством интрактринного механизма.
Вскоре после того, как были выделены FGF1 и FGF2, выделили еще пару факторов роста, связывающих гепарин и названных HBGF-1 и HBGF-2; наряду с ними была выделена третья группа факторов роста, вызывающих пролиферации клеток в биопробе, содержащей в себе эндотелиальные клетки кровеносного сосуда. Эти факторы роста получили название ECGF1 и ECGF2. Эти белки оказались идентичными кислому и основному факторам роста фибробластов, описанным Господаровичем (Gospodarowicz).
Функции
Факторы роста фибробластов — многофункциональные белки с большим набором эффектов; чаще всего они являются митогенами, но также оказывают регуляторное, структурное и эндокринное воздействие. Другое их название — «плюрипотентные» факторы роста, связано с их разнородным воздействием на многие типы клеток.[13][14] Что касается FGF, четыре подтипа рецепторов могут активироваться более чем двадцатью разными лигандами.
Функции FGFs в процессах развития включают мезодермальную индукцию, правильную цефализацию в процессе эмбриогенеза[6] , развитие конечностей, формирование нейрулы[15] и развитие нервной системы, а в зрелых тканях/системах — регенерацию тканей, рост кератиноцитов и заживление ран.
Факторы роста фибробластов имеют особое значение для нормального онтогенеза как позвоночных, так и беспозвоночных, и любые отклонения от нормы в их действиях ведут к ряду дефектов в развитии.[16][17][18][19]
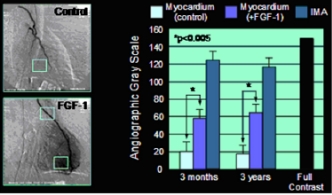
Одна из важных функций FGF1 и FGF2 — это стимуляция роста эндотелиальных клеток и организация их в трубчатую структуру. Таким образом, они ускоряют ангиогенез, рост новых кровеносных сосудов из уже существующей сосудистой сети. FGF1 и FGF2 являются более мощными ангиогенными факторами, нежели фактор роста эндотелия сосудов (VEGF) или фактор роста тромбоцитов (PDGF).[20] Помимо стимулирования роста кровеносных сосудов, FGFs являются важными участниками процесса заживления ран. FGF1 и FGF2 стимулируют ангиогенез и рост фибробластов, которые вызывают рост грануляционной ткани, заполняющей полость раны в начале заживления. FGF7 и FGF10 (также известные как факторы роста кератиноцитов KGF и KGF2, соответственно) дают толчок восстановлению поврежденной кожи и слизистой оболочки за счет стимуляции пролиферации, перемещения и дифференцировки эпителиальных клеток.
Во время развития центральной нервной системы FGFs играют важную роль в нейрогенезе, росте аксонов и дифференцировке. FGFs также важны для защиты зрелого мозга. Таким образом, FGFs являются решающим фактором выживания нейронов как во время эмбрионального развития, так и в период взрослой жизни.[21] Нейрогенез у взрослых млекопитающих в гиппокампе, например, во многом зависит от FGF-2. К тому же FGF-1 и FGF-2, похоже, участвуют в регуляции синаптической пластичности и процессах, отвечающих за обучение и запоминание, по крайней мере, в гиппокампе.[22]
Большинство FGFs — секретируемые белки, которые связывают гепаринсульфат, и поэтому они могут закрепляться на внеклеточном матриксе, содержащем гепарансульфатпротеогликан. Это позволяет им действовать локально как паракринные факторы. Тем не менее, белки подсемейства FGF19 (включающего в себя FGF19, FGF21 и FGF23), которые менее прочно связываются с гепаринсульфатом, могут участвовать в эндокринной сигнализации, действуя на ткани, находящиеся на большом расстоянии, таких как кишечная, печеночная, почечная, жировая и костная. Например, FGF19 производится кишечными клетками, но воздействует на клетки печени, экспрессирующие FGFR4, снижая активность ключевых генов, участвующих в синтезе желчных кислот); FGF23 производится костной тканью, но воздействуют на FGFR1- экспрессирующие клетки почек для регуляции синтеза витамина D, что в свою очередь влияет на гомеостаз кальция[9].
Структура
Была определена трехмерная структура HBGF1; она оказалась сходной со структурой интерлейкина 1-бета, оба семейства имеют ту же структуру из 12-полосного бета-листа; складчатые бета-слои располагаются в виде трех одинаковых лопастей вокруг центральной оси, при этом шесть полом формируют встречно-параллельную бета-бочку.[23][24][25] Бета-листы весьма консервативны, и кристаллическая структура весьма сходна в этих участках. Промежуточные петли менее сходны — петля между бета-слоями 6 и 7 немного длиннее, чем в интерлейкине1-бета.
См. также
Примечания
- ↑ Finklestein S.P., Plomaritoglou A. Growth factors // Head Trauma: Basic, Preclinical, and Clinical Directions / Miller L.P., Hayes R.L., eds. Co-edited by Newcomb J.K.. — New York : Wiley, 2001. — P. 165–187. — ISBN 0-471-36015-5.
- ↑ Blaber M, DiSalvo J, Thomas KA (February 1996). “X-ray crystal structure of human acidic fibroblast growth factor”. Biochemistry. 35 (7): 2086—94. DOI:10.1021/bi9521755. PMID 8652550. Используется устаревший параметр
|month=(справка) - ↑ Ornitz DM, Itoh N (2001). “Fibroblast growth factors”. Genome Biol. 2 (3): reviews3005.1—reviews3005.12. DOI:10.1186/gb-2001-2-3-reviews3005. PMC 138918. PMID 11276432.
- ↑ Olsen SK, Garbi M.; et al. (2003). “Fibroblast growth factor (FGF) homologous factors share structural but not functional homology with FGFs”. J. Biol. Chem. 278 (36): 34226—36. DOI:10.1074/jbc.M303183200. PMID 12815063.
- ↑ Itoh N, Ornitz DM (January 2008). “Functional evolutionary history of the mouse Fgf gene family”. Dev. Dyn. 237 (1): 18—27. DOI:10.1002/dvdy.21388. PMID 18058912. Используется устаревший параметр
|month=(справка) - 1 2 Koga C, Adati N, Nakata K, Mikoshiba K, Furuhata Y, Sato S, Tei H, Sakaki Y, Kurokawa T (August 1999). “Characterization of a novel member of the FGF family, XFGF-20, in Xenopus laevis”. Biochemical and Biophysical Research Communications. 261 (3): 756—65. DOI:10.1006/bbrc.1999.1039. PMID 10441498. Используется устаревший параметр
|month=(справка) - ↑ Kirikoshi H, Sagara N, Saitoh T, Tanaka K, Sekihara H, Shiokawa K, Katoh M (August 2000). “Molecular cloning and characterization of human FGF-20 on chromosome 8p21.3-p22”. Biochemical and Biophysical Research Communications. 274 (2): 337—43. DOI:10.1006/bbrc.2000.3142. PMID 10913340. Используется устаревший параметр
|month=(справка) - ↑ Fukumoto S (March 2008). “Actions and mode of actions of FGF19 subfamily members”. Endocr. J. 55 (1): 23—31. DOI:10.1507/endocrj.KR07E-002. PMID 17878606. Используется устаревший параметр
|month=(справка) - 1 2 Degirolamo C., Sabbà C., Moschetta A. Therapeutic potential of the endocrine fibroblast growth factors FGF19, FGF21 and FGF23 (англ.) // Nat. Rev. Drug Discov.. — 2016. — Vol. 15. — P. 51-69. — DOI:10.1038/nrd.2015.9.
- ↑ Armelin HA (September 1973). “Pituitary extracts and steroid hormones in the control of 3T3 cell growth”. Proc. Natl. Acad. Sci. U.S.A. 70 (9): 2702—6. Bibcode:1973PNAS...70.2702A. DOI:10.1073/pnas.70.9.2702. PMC 427087. PMID 4354860. Используется устаревший параметр
|month=(справка) - ↑ Gospodarowicz D (1974). “Localisation of a fibroblast growth factor and its effect alone and with hydrocortisone on 3T3 cell growth”. Nature. 249 (453): 123—7. Bibcode:1974Natur.249..123G. DOI:10.1038/249123a0. PMID 4364816.
- ↑ Arese M, Chen Y.; et al. (1999). “Nuclear activities of basic fibroblast growth factor: potentiation of low-serum growth mediated by natural or chimeric nuclear localization signals”. Mol. Biol. Cell. 10 (5): 1429—44. PMC 25296. PMID 10233154.
- ↑ Vlodavsky I, Korner G, Ishai-Michaeli R, Bashkin P, Bar-Shavit R, Fuks Z (1990). “Extracellular matrix-resident growth factors and enzymes: possible involvement in tumor metastasis and angiogenesis”. Cancer Metastasis Rev. 9 (3): 203—26. DOI:10.1007/BF00046361. PMID 1705486.
- ↑ Green PJ, Walsh FS, Doherty P (1996). “Promiscuity of fibroblast growth factor receptors”. BioEssays. 18 (8): 639—46. DOI:10.1002/bies.950180807. PMID 8760337.
- ↑ Böttcher RT, Niehrs C. (2005). “Fibroblast growth factor signaling during early vertebrate development”. Endocr. Rev. 26 (1): 63—77. DOI:10.1210/er.2003-0040. PMID 15689573.
- ↑ Amaya E, Musci T.J. and Kirschner M.W. (1991). “Expression of a dominant negative mutant of the FGF receptor disrupts mesoderm formation in Xenopus embryos”. Cell. 66 (2): 257—270. DOI:10.1016/0092-8674(91)90616-7. PMID 1649700.
- ↑ Borland C.Z., Schutzman J.L. and Stern M.J. (2001). “Fibroblast growth factor signaling in Caenorhabditis elegans”. BioEssays. 23 (12): 1120—1130. DOI:10.1002/bies.10007. PMID 11746231.
- ↑ Coumoul X. and Deng C.X. (2003). “Roles of FGF receptors in mammalian development and congenital diseases”. Birth Defects Res C Embryo Today. 69 (4): 286—304. DOI:10.1002/bdrc.10025. PMID 14745970.
- ↑ Sutherland D, Samakovlis C . and Krasnow M.A. (1996). “Branchless encodes a Drosophila FGF homolog that controls tracheal cell migration and the pattern of branching”. Cell. 87 (6): 1091—1101. DOI:10.1016/S0092-8674(00)81803-6. PMID 8978613.
- ↑ Vlodavsky Cao R, Bråkenhielm E, Pawliuk R, Wariaro D, Post MJ, Wahlberg E, Leboulch P, Cao Y (2003). “Angiogenic synergism, vascular stability and improvement of hind-limb ischemia by a combination of PDGF-BB and FGF-2”. Nature Med. 9 (5): 604—13. DOI:10.1038/nm848. PMID 12669032.
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/12845521, Reuss B, von Bohlen und Halbach O. 2003. Fibroblast growth factors and their receptors in the central nervous system. Cell Tissue Res 313: 139—157.
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/20581332, Zechel S, Werner S, Unsicker K, von Bohlen und Halbach O. 2010. Expression and functions of fibroblast growth factor 2 (FGF-2) in hippocampal formation. Neuroscientist 16: 357—373.
- ↑ Murzin AG, Lesk AM, Chothia C (January 1992). “beta-Trefoil fold. Patterns of structure and sequence in the Kunitz inhibitors interleukins-1 beta and 1 alpha and fibroblast growth factors”. J. Mol. Biol. 223 (2): 531—43. DOI:10.1016/0022-2836(92)90668-A. PMID 1738162. Используется устаревший параметр
|month=(справка) - ↑ Eriksson AE, Cousens LS, Weaver LH, Matthews BW (April 1991). “Three-dimensional structure of human basic fibroblast growth factor”. Proc. Natl. Acad. Sci. U.S.A. 88 (8): 3441—5. Bibcode:1991PNAS...88.3441E. DOI:10.1073/pnas.88.8.3441. PMC 51463. PMID 1707542. Используется устаревший параметр
|month=(справка) - ↑ Gimenez-Gallego G, Rodkey J, Bennett C, Rios-Candelore M, DiSalvo J, Thomas K (December 1985). “Brain-derived acidic fibroblast growth factor: complete amino acid sequence and homologies”. Science. 230 (4732): 1385—8. Bibcode:1985Sci...230.1385G. DOI:10.1126/science.4071057. PMID 4071057. Используется устаревший параметр
|month=(справка)
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .