Эту страницу предлагается объединить со страницей Ривароксабан. |
Ривароксабан (Ксарелто, BAY 59-7939, англ. Rivaroxaban, Xarelto) - антикоагулянт орального применения. Он широко используется для того чтобы предотвратить свертывание крови. Первоначально был разработан компанией Байер. В Соединенных Штатах он продается компанией Янссен Фармацевтика Это первый доступный активный прямой ингибитор фактора Ха перорального применения. Максимальное ингибирование фактора Ха возникает через четыре часа после приёма дозы. Эффект длится около 8-12 часов, но активность фактора XA не возвращается к норме в течение 24 часов, поэтому достаточно его принимать один раз в сутки.
Ривароксабан был запатентован в США в 2007 году, одобрен для медицинского применения в 2011 году, патентная защита истекает в 2020 году.[1]
Медицинское применение
У пациентов с неклапанной фибрилляцией предсердий препарат столь же эффективен, как варфарин в предотвращении негеморрагических инсультов и тромбоэмболии.[2] Применение Ривароксабана связано со сниженным риском сильных и смертельных кровотечений, чем варфарин. Хотя ривароксабан и связан с более высокой частотой кровотечений в желудочно-кишечном тракте.[3]
В июле 2012 года британский Национальный институт здравоохранения и медицины рекомендовал ривароксабан для профилактики и лечения венозной тромбоэмболии.[4]
Побочные эффекты
Наиболее серьезный побочный эффект это кровотечения, включая тяжелые внутренние кровотечения.[5][6][7] Применение Ривароксабана связано со сниженным риском сильных и смертельных кровотечений, чем варфарин, но связан с более высокой частотой кровотечений в ЖКТ. В настоящее время не существует антидота для ривароксабана (в отличие от варфарина, действие которого может быть инвертировано с помощью витамина К и протромбинового комплексного концентрата), это означает, что серьезным кровотечением может быть трудно управлять.
В октябре 2014 года, компания Портола Фармасьютикалз завершила фазы I и II клинических испытаний для andexanet Альфа в качестве антидота для ингибиторов фактора Ха с несколько побочных эффектов, и начала исследования III фазы.[8][9] Andexanet Альфа, как ожидается, будет утвержден в 2016 году.[10] В 2017 году соединение ещё не было одобрено FDA.
В 2015 году пост-маркетинговые исследования выявили токсичность для печени, и показали необходимость дальнейших исследований для количественной оценки риска.[11][12] Препарат противопоказан людям с серьезными заболеваниями печени и терминальной стадии почечной болезни, при которых исследований не проводилось.
Ривароксабан в индивидуальной упаковке имеет предупреждение, о том, что людям использующим препарат не следует прекращать его применения до консультации с врачом, так как это может увеличить риск инсульта.[13]
В 2015 году на ривароксабан приходится наибольшее количество зарегистрированных случаев серьезных осложнений среди регулярно контролируемых FDA лекарств.[14]
Механизм действия
Ривароксабан подавляет свободный фактор Ха и фактор Ха связанный в комплекс протромбиназы.[15] Это высокоселективный прямой ингибитор фактора Ха с пероральной биодоступностью и быстрым началом действия. Ингибирование фактора Ха прерывает внутренние и внешние пути свертывания крови, препятствует образованию тромбина и развитию тромбов. Ривароксабан не подавляет тромбин (активированный фактор II) и не оказывает никакого влияния на тромбоциты.[16] Это позволяет легко корректировать дозы в антикоагулянтной терапии и отслеживать коагуляцию [16] , а также избегать ограничений в питании.[10]
Нефракционированный гепарин, низкомолекулярный гепарин и фондапаринукс также ингибируют активность фактора Ха, но косвенно, путем связывания циркулирующего антитромбина (АТ III). Принимая во внимание, что орально активный варфарин, аценокумарол являются антагонистами витамина К уменьшая количество факторов свертывания крови, включая фактор X.[17] Ривароксабан имеет предсказуемую фармакокинетику у широкого спектра пациентов (возраст, пол, вес, раса) и имеет линейную кривую доза-эффект в восьмикратном диапазоне доз (5-40 мг).[18]
Химия
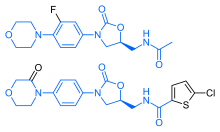
Ривароксабан имеет поразительное структурное сходство с антибиотиками группы линезолида: оба препарата имеют те же оксазолидинон-производные основные структуры. Соответственно, ривароксабан изучался на возможную противомикробную активность и митохондриальную токсичность, которая является известным осложнением долгосрочного применения линезолида. Исследования показали, что ни ривароксабан, ни его метаболиты не обладают антибактериальным действием против грам-положительных бактерий. Что касается митохондриальной токсичности, то в исследованиях In vitro, опубликованных до 2008 года выявленный риск был низким.[19]
Антидот
Специфическим антидотом ривороксабана является препарат Андекса (рекомбинантный инактивированный фактор Xa).
Общество и культура
Экономика
Использование ривароксабана в 70 раз чаще варфарина, по данным Express Scripts Holding Co, крупнейшей в США компанией по работе с аптеками.[10] В 2016 году, Байер утверждал, что препарат был лицензирован в 130 странах и более 23 миллионов пациентов прошли лечение.[20]
Одобрение
В сентябре 2008 года, Министерство здравоохранения Канады выдало регистрационное удостоверение на ривароксабан для профилактики венозной тромбоэмболии у людей, которые прошли замену тазобедренного сустава или полное эндопротезирование коленного сустава.[21] В том же месяце Европейская комиссия также выдано регистрационное удостоверение ривароксабана для профилактики венозной тромбоэмболии у взрослых пациентов, перенесших плановые бедра и коленного сустава.[22]
На 1 июля 2011 года, в США продуктов питания и медикаментов (FDA) одобрила ривароксабан для профилактики тромбоза глубоких вен (ТГВ), который может привести к тромбоэмболии легочной артерии (ТЭЛА), у взрослых, перенесших эндопротезирование тазобедренного и коленного сустава.[23]
4 ноября 2011 года FDA США одобрило ривароксабан для профилактики инсульта у пациентов с неклапанной фибрилляцией предсердий.[24]
Исследования
Исследователи из Школы медицины Университета Дьюка были обвинены в сокрытии клинических данных, используемых для оценки ривароксабана.[25] Они проводили клинические испытания ривароксабана ROCKET AF.[26] В клиническом исследовании, опубликованном в 2011 году в медицинском журнале в Новой Англии [27] которое возглавил Роберт Калиффи, (представитель FDA[28])[27] нашли что ривароксабан, более эффективен, чем варфарин в снижении вероятности ишемических инсультов у пациентов с фибрилляцией предсердий.[27] Валидность исследования была поставлена под вопрос в 2014 году, когда фармацевтическими компаниями Байер и Джонсон и Джонсон установлено, что использованные приборы мониторинга крови INRatio не функционируют должным образом[25][26]. Последующий анализ исследований Школы медицины Университета Дьюка, опубликованные в феврале 2016 года обнаружил, что это не оказало существенного влияния на эффективность и безопасность испытаний.[29]
См. также
- Апиксабан
- Бетриксабан
- Дарексабан (YM150)
- Эдоксабан (DU-176b)
- Андекса
Ссылки
- ↑ Generic Xarelto Availability - Drugs.com (англ.), Drugs.com. Проверено 8 апреля 2018.
- ↑ Gómez-Outes, A; Terleira-Fernández, AI; Calvo-Rojas, G; Suárez-Gea, ML; Vargas-Castrillón, E (2013). “Dabigatran, Rivaroxaban, or Apixaban versus Warfarin in Patients with Nonvalvular Atrial Fibrillation: A Systematic Review and Meta-Analysis of Subgroups”. Thrombosis. 2013: 640723. DOI:10.1155/2013/640723. PMC 3885278. PMID 24455237.
- ↑ Brown DG, Wilkerson EC, Love WE (March 2015). “A review of traditional and novel oral anticoagulant and antiplatelet therapy for dermatologists and dermatologic surgeons”. Journal of the American Academy of Dermatology. 72 (3): 524—34. DOI:10.1016/j.jaad.2014.10.027. PMID 25486915.
- ↑ NICE guidance TA261 NICE guidance TA261. National Institute for Health and Clinical Excellence, July 2012
- ↑ Medication Guide--Xarelto. U.S. Food and Drug Administration. Проверено 1 сентября 2014.
- ↑ Xarelto Side Effects. WebMD. Проверено 1 сентября 2014.
- ↑ Xarelto Side Effects Center. RxList. Проверено 1 сентября 2014.
- ↑ Possible Antidote Could Help Blood Thinner Patients In Bleeding Emergencies. DrugNews. Проверено 20 августа 2015.
- ↑ Mo Y, Yam FK (Feb 2015). “Recent advances in the development of specific antidotes for target-specific oral anticoagulants”. Pharmacotherapy. 35 (2): 198—207. DOI:10.1002/phar.1532. PMID 25644580.
- 1 2 3 Bill Berkrot New blood thinner 'antidote' to help doctors move past warfarin. Reuters (December 23, 2015).
- ↑ Raschi, Emanuel; Poluzzi, Elisabetta; Koci, Ariola; Salvo, Francesco; Pariente, Antoine; Biselli, Maurizio; Moretti, Ugo; Moore, Nicholas; De Ponti, Fabrizio (2015-08-01). “Liver injury with novel oral anticoagulants: assessing post-marketing reports in the US Food and Drug Administration adverse event reporting system”. British Journal of Clinical Pharmacology. 80 (2): 285—293. DOI:10.1111/bcp.12611. ISSN 1365-2125. PMC 4541976. PMID 25689417.
- ↑ Russmann, Stefan; Niedrig, David F.; Budmiger, Mathias; Schmidt, Caroline; Stieger, Bruno; Hürlimann, Sandra; Kullak-Ublick, Gerd A. (2014-08-01). “Rivaroxaban postmarketing risk of liver injury”. Journal of Hepatology. 61 (2): 293—300. DOI:10.1016/j.jhep.2014.03.026. ISSN 1600-0641. PMID 24681117.
- ↑ XARELTO (rivaroxaban) label. U.S. Food and Drug Association.
- ↑ ISMP Ranks Xarelto Most Dangerous Drug in the United States. DrugNews. DrugNews. Проверено 10 августа 2016.
- ↑ Roehrig S, Straub A, Pohlmann J, et al. (September 2005). “Discovery of the novel antithrombotic agent 5-chloro-N-({(5S)-2-oxo-3- [4-(3-oxomorpholin-4-yl)phenyl]-1,3-oxazolidin-5-yl}methyl)thiophene- 2-carboxamide (BAY 59-7939): an oral, direct factor Xa inhibitor”. Journal of Medicinal Chemistry. 48 (19): 5900—8. DOI:10.1021/jm050101d. PMID 16161994.
- 1 2
- ↑ Turpie AG (January 2008). “New oral anticoagulants in atrial fibrillation”. European Heart Journal. 29 (2): 155—65. DOI:10.1093/eurheartj/ehm575. PMID 18096568.
- ↑ Eriksson BI, Borris LC, Dahl OE, et al. (November 2006). “A once-daily, oral, direct Factor Xa inhibitor, rivaroxaban (BAY 59-7939), for thromboprophylaxis after total hip replacement”. Circulation. 114 (22): 2374—81. DOI:10.1161/CIRCULATIONAHA.106.642074. PMID 17116766.
- ↑ European Medicines Agency. CHP Assessment Report for Xarelto (EMEA/543519/2008) (2008). Проверено 11 июня 2009. (недоступная ссылка)
- ↑ Bayer comments on article in The British Medical Journal (BMJ) regarding Xarelto. Bayer AG Communications, Government Relations & Corporate Brand (29 September 2016).
- ↑ Bayer (2008-09-16). Bayer's Xarelto Approved in Canada. Пресс-релиз. Проверено 2010-01-31.
- ↑ Bayer (2008-02-10). Bayer’s Novel Anticoagulant Xarelto now also approved in the EU. Пресс-релиз. Проверено 2010-01-31.
- ↑ Janssen Pharmaceutica (2011-07-01). FDA Approves XARELTO® (rivaroxaban tablets) to Help Prevent Deep Vein Thrombosis in Patients Undergoing Knee or Hip Replacement Surgery. Пресс-релиз. Проверено 2011-07-01.
- ↑ FDA approves Xarelto to prevent stroke in people with common type of abnormal heart rhythm, U.S. Food and Drug Association (4 November 2011). Проверено 27 апреля 2016.
- 1 2 Document Claims Drug Makers Deceived a Top Medical Journal. The New York Times. The New York Times. Проверено 3 мая 2016.
- 1 2 Duke clinical trial under scrutiny in drug case. The Chronicle. Duke Student Publishing Company.
- 1 2 3 Rivaroxaban versus Warfarin in Nonvalvular Atrial Fibrillation. The New England Journal of Medicine. Massachusetts Medical Society.
- ↑ Meet Robert M. Califf, M.D., Commissioner of Food and Drugs. U.S. Food and Drug Administration. U.S. Food and Drug Administration. Проверено 3 мая 2016.
- ↑ Point-of-Care Warfarin Monitoring in the ROCKET AF Trial. Massachusetts Medical Society (February 3, 2016).
Внешние ссылки
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .