| Ацетилацетон | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
2,4-пентандион |
| Сокращения | асас |
| Традиционные названия | ацетилацетон |
| Хим. формула | СН3СОСН2СОСН3 |
| Рац. формула | C5H8O2 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 100,13 г/моль |
| Плотность | 0,98 г/см³ |
| Термические свойства | |
| Т. плав. | -23 °C |
| Т. кип. | 140 °C |
| Т. всп. | 34 °C |
| Т. свспл. | 340 °C |
| Давление пара | 9 гПа |
| Химические свойства | |
| pKa | 9 |
| Растворимость в воде | 16 г/100 мл |
| Растворимость в орг. растворители | смешивается |
| Оптические свойства | |
| Показатель преломления | 1,4609 |
| Классификация | |
| Рег. номер CAS | 123-54-6 |
| PubChem | 31261 |
| Рег. номер EINECS | 204-634-0 |
| SMILES | |
| InChI | |
| ChEBI | 14750 |
| ChemSpider | 29001 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Ацетилацетон (диацетилметан, пентан-2,4-дион) СН3-СО-СН2-СО-СН3 — органическое соединение, относящееся к классу кетонов с формулой C5H8O2. Этот дикетон имеет формальное название 2,4-пентандион. Он является прекурсором для синтеза ацетилацетонатов (асас), распространенный бидентантный лиганд. Также является билдинг блоком для синтеза гетероциклических соединений.
Свойства
Бесцветная жидкость с запахом ацетона и уксусной кислоты.
Кето и енольная форма ацетилацетона сосуществуют в растворе; эти формы являются таутомерами. C2v симметрия для енола показанного на левой части схема была проверена разными методами в том числе и микроволновой спектроскопией [1] Водородная связь в еноле уменьшает стерическое отталкивание между карбонильными группами. В газовой фазе К, точнее её отрицательный логарифм pKa равен 11,7. Константа равновесия стремится к увеличению в неполярных растворителях: циклогексан — 42, толуол — 10, ТГФ 7.2, ДМСО (рK=2), и в воде (рK=0.23).[2] Енольная форма является винилогическим аналогом карбоксильной кислоты.
Получение
Ацетилацетон получается индустриально термической перегруппировкой изопропенил ацетата. [3]
- CH2C(CH3)OC(O)Me → MeC(O)CH2C(O)Me
Лабораторные пути к ацетилацетону начинаются на ацетоне. Ацетон и уксусный ангидрид при добавке BF3 в качестве катализатора:
- (CH3CO)2O + CH3C(O)CH3 → CH3C(O)CH2C(O)CH3
Второй синтез включает катализируемая основаниями конденсация ацетона и этилацетата, с последующим подкислением.
- NaOEt + EtO2CCH3 + CH3C(O)CH3 → NaCH3C(O)CHC(O)CH3 + 2 EtOH
- NaCH3C(O)CHC(O)CH3 + HCl → CH3C(O)CH2C(O)CH3 + NaCl
Благодаря лёгкости этих синтезов известно много аналогов ацетилацетонатов. Некоторые примеры включают C6H5C(O)CH2C(O)C6H5 (dbaH) и (CH3)3CC(O)CH2C(O)CC(CH3)3. Гексафторацетилацетонаты (F3CC(O)CH2C(O)CF3) широко используются для получения летучих комплексов металлов.
Ацетилацетонат анион
Ацетилацетонат анион, C5H7O2−, является сопряженным основанием 2,4-пентандиона. Он не существует свободно в виде аниона в растворе, напротив он связан с соответствующим катионом таким как Na+. На практике, существование свободного аниона, обычно сокращаемого acac−, только удобная модель. Натрий ацетилацетонат может быть получен депротонированием ацетилацетона гидроксидом натрия в смеси вода-метанол.
Координационная химия
С ионами металлов ацетилацетон дает прочные комплексные соединения, которые используют в аналитической химии для определения и разделения бериллия, меди, хрома, железа и других металлов; в радиохимии — для выделения радиоактивных изотопов.
Ацетилацетонат анион образует комплексы с многими ионами переходных металлов, где оба атома кислорода связаны с металлом, образуя шестичленные хелатные комплексы. Некоторые примеры, включая Mn(acac)3,[4], VO(acac)2, Fe(acac)3, and Co(acac)3. Любой комплекс формулы M(acac)3 хиральный (имеет несовместимость со своим отражением в зеркале). Дополнительно комплексы M(acac)3 могут быть восстановлены; электрохимически глубина восстановления зависит от растворителя и металлического центра. [5] Бис и трис комплексы типа M(acac)2 и M(acac)3 в основном растворимы в органических растворителях, в противоположность соответствующим галидам. Важное применение включает в себя использование их в 1Н ЯМР в качестве «смещающего реагента» и в качестве катализаторов в органическом синтезе, и прекурсоров к промышленным катализаторам гидроформилирования. C5H7O2− соединения в некоторых случаях происходит через центральный углеродный атом; этот тип связывания более характерен для third-row переходных металлов таких как платина(II) и иридий(III).
Ацетилацетонаты металлов
Хром(III) ацетилацетонат
Cr(acac)3 используется как спин релаксационный агент для увеличения чувствительности в количественной углерод-13 ЯМР спектроскопии.[6]
Меди(II) ацетилацетонат
Cu(acac)2, получается обработкой ацетилацетона водным раствором Cu(NH3)42+ и доступен коммерчески, каталлизирует сочетание или реакции переноса карбена.
Медь(I) ацетилацетонат
В отличие от медь(II) производных, медь(I) ацетилацетонат чувствителен к воздуху. Он используется в качестве катализатора реакции Михаэля[7]
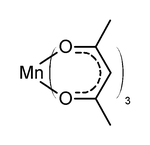
Марганец(III) ацетилацетонат

Марганец(III) ацетилацетонат, Mn(acac)3, одноэлектронный окислитель, используется для сочетания фенолов. Его получают прямой реакцией ацетилацетона и калия перманганатом. В терминах электронной структуры, Mn(acac)3 высокоспиновый. Эта искаженная октаэдральная структра отражает геометрическое искривление благодаря эффекту Яна — Теллера. Две наиболее общие структуры для этого комплекса включает один с тетрэдральным увеличением и один с тетрэдральным сжатием. Для увеличения две Mn-O связи составляет 2.12 Å в то время как другие четверо 1.93 Å. Для сжатия, две Mn-O связи составляют 1.95 Å и четверо других 2.00 Å. Эффект тетраэдрального увеличения заметно более важен чем эффект тетраэдрального сжатия.
Никель(II) ацетилацетонат

Никель(II) ацетилацетонат это не Ni(acac)2, а тример [Ni(acac)2]3. Он изумрудно-зелёного цвета твёрдое вещество, которое нерастворимо в бензоле. Широко используется для получения Ni(O)комплекса. Под действием воздуха [Ni(acac)2]3 переходит в зеленоватый мономерный гидрат.
Ванадил ацетилацетонат
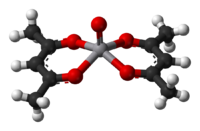
Ванадил ацетилацетонат сине-зелёный комплекс с формулой V(O)(acac)2. Плохо растворим в воде. Хорошо растворим в органических растворителях. Водный раствор окрашивает в тёмно-зелёный цвет. Он полезен в эпоксидировании аллильных спиртов.
Цинк ацетоноацетат
Моногидро комплекс Zn(acac)2H2O (m.p. 138—140 °C) пентокоординатный, принимает форму квадратной пирамиды.[8] Дегидратация этих веществ даёт гигроскопическое сухое производное (m.p. 127 °C).[9] Этот более летучее производное использовалось как прекурсор для плёнок ZnO
Иридий ацетоноацетат
Оба иридий(I) и иридий(III) образует стабильные ацетилацетонатные комплексы. Ir(III) производные включая trans-Ir(acac)2(CH(COMe)2)(H2O) и более распространенный D3-symmetric Ir(acac)3. Производные с С-связью является прекурсором для гомогенных катализаторов для C-H активирования и соответствующих химий.[10][11] Иридий(I) производные включают планарно-квадратный Ir(acac)(CO)2 (C2v-симметрия).
Алюминий(III) ацетилацетонат
Al(C5H7O2)n, или сокращённо Al(acac)3 Образует кристаллический желтоватый осадок при прямой реакции ацетилацетона с растворимой солью алюминия в щелочной среде при нагревании.
C-связанные ацетилацетонаты
C5H7O2− в некоторых случаях также связывает металл через центральный атом углерода (C3); этот способ связывания характерен для металлов третьего переходного ряда, таких как платина(II) и иридий(III). Комплекс Ir(acac)3 и соответствующий аддукт с основанием Льюиса Ir(acac)3L (L = an амин) содержат один углеродно-связанный acac лиганд. ИК-спектры О-связанных ацетилацетонатов характеризуется относительно малоэнергетическим νCO линиями при 1535 см−1, тогда как в углеродно-связанном ацетилацетонате наблюдается линия поглощения νC=O при 1655 см−1, характерная для кетонов.
Другие реакции ацетилацетона
- Депротонирование: очень сильные основания могут дважды депротонировать ацетилацетон, начиная с С3, а также С1. Образующееся вещество может быть проалкилировано по атому C-1.
- Прекурсор для синтеза гетероциклов: Ацетилацетон — многофункциональный прекурсор гетероциклов. Так, гидразин даёт при конденсации с ацетилацетонами замещенные пиразолы, а мочевина — пиримидины.
- Прекурсор соответствующих имино-лигандов: ацетилацетон конденсируется с аминами, давая моно- и ди-кетимины, в которых один либо два атома кислорода ацетилацетона, соответственно, замещаются на группу NR (где R = арил, алкил).
- Фермент ацетилацетона диоксигеназа разрывает связь углерод-углерод с образованием ацетата и 2-оксопропаналя. Фермент Fe(II) зависим, но было доказано соединение также с цинком. Деградация ацетилацетона была охарактеризивана в бактерии johnsonii.[12]
- C5H8O2 + O2 → C2H4O2 + C3H4O2
- Арилирование: ацетилацетонат замещает галиды из обычной галогенозамещённой бензойной кислоты. Реакция катализируется медью.
- 2-BrC6H4CO2H + NaC5H7O2 → 2-(CH3CO)2HC)-C6H4CO2H + NaBr
Безопасность
КПВ 2.4-11.6 %
См. также
Примечания
- ↑ W. Caminati, J.-U. Grabow (2006). “The C2v Structure of Enolic Acetylacetone”. Journal of the American Chemical Society. 128 (3): 854—857. DOI:10.1021/ja055333g.
- ↑ Solvents and Solvent Effects in Organic Chemistry, Christian Reichardt Wiley-VCH; 3 edition 2003 ISBN 3-527-30618-8
- ↑ Hardo Siegel, Manfred Eggersdorfer «Ketones» in Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, 2002, Wienheim. DOI:10.1002/14356007.a15_077
- ↑ B. B. Snider, «Manganese(III) Acetylacetonate» in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. DOI:10.1002/047084289
- ↑ W. Fawcett, M. Opallo (1992). “Kinetic parameters for heterogeneous electron transfer to tris(acetylacetonato)manganese(III) and tris(acetylacetonato)iron(III) in aproptic solvents”. Journal of Electroanalytical Chemistry. 331: 815—830. DOI:10.1016/0022-0728(92)85008-Q.
- ↑ Caytan, Elsa; Remaud, Gerald S.; Tenailleau, Eve; Akoka, Sergehjhk,j (2007). “Precise and accurate quantitative 13C NMR with reduced experimental time”. Talanta. 71 (3): 1016—1021. DOI:10.1016/j.talanta.2006.05.075.
- ↑ E. J. Parish, S. Li «Copper(I) Acetylacetonate» in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. DOI:10.1002/047084289X.rc203
- ↑ H. Montgomery and E. C. Lingafelter «The crystal structure of monoaquobisacetylacetonatozinc» Acta Crystallographica (1963), volume 16, pp. 748—752. doi:10.1107/S0365110X6300195X.
- ↑ G. Rudolph and M. C. Henry «Bis(2,4-Pentanedionato)zinc (Zinc Acetylacetonate)» Inorganic Syntheses, 1967, volume X, pp. 74-77.
- ↑ Bennett, M. A.; Mitchell, T. R. B. «γ-Carbon-bonded 2,4-pentanedionato complexes of trivalent iridium» Inorganic Chemistry 1976, volume 15, pp. 2936-8. DOI:10.1021/ic50165a079
- ↑ Bhalla, G.; Oxgaard, J.; Goddard, W. A., II, and Periana, R. A., «Hydrovinylation of Olefins Catalyzed by an Iridium Complex via CH Activation», Organometallics, 2005, 24, 5499-5502.DOI:10.1021/om050614i
- ↑ Straganz, G.D., Glieder, A., Brecker, L., Ribbons, D.W. and Steiner, W. «Acetylacetone-Cleaving Enzyme Dke1: A Novel C-C-Bond-Cleaving Enzyme.» Biochem. J. 369 (2003) 573—581 DOI:10.1042/BJ20021047
Для улучшения этой статьи желательно: |
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .