| Фторид фосфора | |
|---|---|
 | |
 | |
| Общие | |
| Хим. формула | F₃P |
| Рац. формула | PF3 |
| Внешний вид | бесцветный газ |
| Физические свойства | |
| Молярная масса | 87.968971 г/моль |
| Плотность | 0,00391 г/см³ |
| Термические свойства | |
| Т. плав. | −151.5 °C |
| Т. кип. | −101.8 °C |
| Классификация | |
| Рег. номер CAS | 7783-55-3 |
| PubChem | 62665 |
| Рег. номер EINECS | 232-008-7 |
| SMILES | |
| InChI | |
| RTECS | TH3850000 |
| ChEBI | 30205 |
| ChemSpider | 56416 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Фторид фосфора(III) (англ. Phosphorus trifluoride) — химическое вещество с формулой PF3; газ без цвета и запаха. Ядовит. Медленно реагирует с водой. Преимущественно используется как лиганд в комплексах металлов. В качестве лиганда он связывается аналогично оксиду углерода(II)[1] в карбонилах. Его токсичность как раз обусловлена сходным с монооксидом углерода способом присоединения к железу гемоглобина.
Свойства
Трифторид фосфора подвержен гидролизу, особенно в щелочной среде, но всё же не в такой степени, как соответствующий хлорид. Он не разлагает стекло, за исключением случая нагрева до высоких температур. С горячими металлами образует соответствующие фосфиды и фториды.
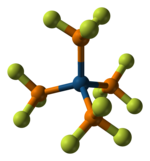
Как лиганд для переходных металлов, PF3 является сильным π-акцептором[2], образующим ряд комплексов с металлами низких степеней окисления, схожих с карбонильными соединениями, но характеризующихся большей устойчивостью. Например, Pd(PF3)4 известен, а Pd(CO)4 — нет[3][4][5]. Такие комплексы обычно приготавливаются из соответствующих карбонильных соединений с выделением монооксида углерода. Однако, металлический никель непосредственно реагирует с PF3 при 100 °C, под давлением 35 МПа, с образованием Ni(PF3)4, аналогичного Ni(CO)4. Cr(PF3)6 может быть получен из дибензолхрома:
- Cr(C6H6)2 + 6PF3 → Cr(PF3)6 + 2C6H6
 |  |
Получение
Трифторид обычно получают из хлорида путём взаимодействия с различными фторидами, например фтороводородом, фторидом кальция, трифторидом мышьяка или фторидом цинка:[6][7][8]
Биологическая активность
Трифторид, как и монооксид углерода, формирует очень устойчивые соединения с железом в гемоглобине, резко снижая концентрацию кислорода в крови.
Токсичность
PF3 высокотоксичен, сравним с фосгеном[9].
Примечания
- ↑ J. Chatt, Nature 165, 637-8 (1950).
- ↑ N. N. Greenwood, A. Earnshaw, Chemistry of the Elements, 2nd ed., Butterworth-Heinemann, Oxford, UK, 1997, p 494
- ↑ D. Nicholls, Complexes and First-Row Transition Elements, Macmillan Press, London, 1973.
- ↑ Kruck, T."Trifluorphosphin-Komplexe von Übergangsmetallen" Angewandte Chemie 1967, volume 79, p 27-43. DOI: 10.1002/ange.19670790104
- ↑ Clark, R. J.; Busch, M. A. «Stereochemical studies of metal carbonylphosphorus trifluoride complexes» Accounts of Chemical Research, 1973, volume 6, pages 246-52.DOI: 10.1021/ar50067a005.
- ↑ A. A. Williams, in Inorganic Syntheses, Vol. V, 95-7 (1946).
- ↑ Nouveau traité de chimie minérale : Tome X, Masson, Paris, France, 1956.
- ↑ Ronald J. Clark, Helen Belefant, Stanley M. Williamson (1990). “Phosphorus Trifluoride”. Inorganic Syntheses. 28: 310—315. DOI:10.1002/9780470132593.ch77.
- ↑ Greenwood, 1997
Литература
- Handbook of Chemistry and Physics, 71st edition, CRC Press, Ann Arbor, Michigan, 1990.
- J. March, Advanced Organic Chemistry, 4th ed., p. 723, Wiley, New York, 1992.
- The Merck Index, 7th edition, Merck & Co, Rahway, New Jersey, USA, 1960.
- A. D. F. Toy, The Chemistry of Phosphorus, Pergamon Press, Oxford, UK, 1973.
Ссылки
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .