| Оксид рутения | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
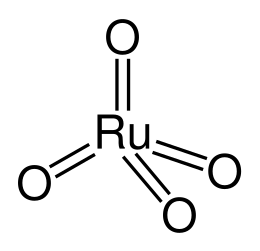
Оксид рутения(VIII) |
| Традиционные названия | Окись рутения(VIII) |
| Хим. формула | RuO4 |
| Физические свойства | |
| Состояние | жёлто-оранжевые кристаллы |
| Молярная масса | 165,07 г/моль |
| Плотность | 3,29 г/см³ |
| Термические свойства | |
| Т. плав. | 25,4; 25,5; 27 °C |
| Т. кип. | |
| Энтальпия образования | -305,2 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 1,710; 2,0320; 2,2574 г/100 мл |
| Классификация | |
| Рег. номер CAS | 20427-56-9 |
| PubChem | 119079 |
| Рег. номер EINECS | 243-813-8 |
| SMILES | |
| InChI | |
| ChemSpider | 106401 |
| Безопасность | |
| Токсичность | Высокотоксичен |
| Пиктограммы СГС |
    |
| NFPA 704 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Оксид рутения(VIII) — неорганическое соединение, оксид металла рутения с формулой RuO4, жёлто-оранжевые кристаллы, умеренно растворимые в воде, образует гидраты.
Получение
- Окисление кислородом воздуха рутения при нагревании:
- Окисление рутения броматом калия:
- Разложение оксида рутения(IV) при нагревании:
- Окисление оксида рутения(IV) кислородом:
- Окисление тетраоксорутената(VI) калия хлором:
Физические свойства
Оксид рутения(VIII) образует жёлто-оранжевые кристаллы.
Тетраоксид рутения — летучее соединение и легко возгоняется[1].
При нагревании выше 100°С разлагается со взрывом.[источник не указан 441 день]
Сильный окислитель, пахнет озоном, со спиртом реагирует со взрывом.
Умерено растворяется в воде, водные растворы являются слабой кислотой p K1 = 11,0.
Химические свойства
- Разлагается при нагревании:
- Является сильным окислителем:
Примечания
- ↑ Откуда мог взяться рутений-106, статья от 24.11.2017 г. с интервью заведующего Лабораторией Института ядерных исследований РАН Б. Жуйкова. Газета «Троицкий вариант — Наука». Н. Демина.
Физиологическое действие
Тетраоксид рутения очень ядовит, летуч, сильный окислитель, поэтому он должен храниться в запаянных ампулах.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4. — 639 с. — ISBN 5-82270-092-4.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .







![{\displaystyle {\mathsf {RuO_{4}+6HCl\ {\xrightarrow {}}\ H_{2}[RuCl_{4}O_{2}]+Cl_{2}\uparrow +2H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/028c38c4ef1d99518de8fd2c21f6a5f7d3851434)
![{\displaystyle {\mathsf {4RuO_{4}+32HCl\ {\xrightarrow {}}\ 2(RuCl_{3}\cdot RuCl_{4}]\downarrow +9Cl_{2}\uparrow +16H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/93dcea741dbb765d62d25da1acd765e7602ad6ba)


